Ressuscitação cardíaca – Terry J Mengert
Terry J. Mengert, MD
Professor of Medicine, University of Washington School of Medicine
Artigo original: Mengert TJ. Cardiac resuscitation. ACP Medicine. 2006;1-14.
[The original English language work has been published by DECKER INTELLECTUAL PROPERTIES INC. Hamilton, Ontario, Canada. Copyright © 2011 Decker Intellectual Properties Inc. All Rights Reserved.]
Tradução: Soraya Imon de Oliveira.
Revisão técnica: Dr. Rodrigo Antônio Brandão Neto.
A parada cardíaca súbita fora do hospital ceifa a vida de mais de 300.000 indivíduos a cada ano, nos Estados Unidos, sendo por isso a principal causa de morte nesse país.1-4 De fato, cerca de 50% de todos os casos de morte cardíaca são súbitos.5 Nos hospitais, pelo menos 370.000 pacientes também sofrem uma parada cardíaca, seguida de tentativa de ressuscitação, que, por sua vez, é bem-sucedida apenas em alguns casos.6 Embora a maioria das vítimas de morte súbita tenha doença arterial coronariana subjacente (70 a 80%), a morte súbita constitui a 1ª manifestação da doença em cerca de metade destes indivíduos.2 Outras causas e fatores contribuidores incluem as anormalidades miocárdicas (p. ex., insuficiência cardíaca crônica ou hipertrofia por causas diversas); anormalidades eletrofisiológicas; cardiopatia valvular; cardiopatia congênita; além de processos patológicos infiltrativos e inflamatórios diversos (p. ex., miocardite, sarcoidose e hemocromatose).7,9
A fisiopatologia que culmina em morte súbita cardíaca é complexa e pouco conhecida. É provável que represente um misto de anormalidades elétricas combinadas a fatores deflagradores funcionais agudos, como a isquemia miocárdica, efeitos do sistema nervoso central e autônomo, anormalidades eletrolíticas e até influências farmacológicas.1 Classicamente, a maioria das mortes súbitas de indivíduos adultos da comunidade é considerada secundária a uma taquicardia ventricular (TV) que sofre degeneração rápida e se transforma em fibrilação ventricular (FV). Em um estudo conduzido na região de Seattle (Estados Unidos), cuja duração foi 10 anos, as diferentes arritmias encontradas em pacientes que sofreram parada cardíaca pré-hospitalar e que presumivelmente estavam associadas a uma doença cardiovascular subjacente foram a FV (45%), assístolia (31%), atividade elétrica sem pulso (AESP – 10%), TV (1%) e outras arritmias (14%).3 Estudos indicam que a incidência de FV fora do hospital diminuiu ao longo dos últimos anos, provavelmente devido à queda da mortalidade por doença arterial coronariana.10 Em um estudo de 4 anos sobre parada cardíaca intra-hospitalar, que envolveu quase 37.000 adultos atendidos em 253 hospitais localizados nos Estados Unidos e Canadá, os ritmos inicialmente identificados foram a assístolia (40%), AESP (24%), ritmos desconhecidos não documentados (22%) e FV ou TV sem pulso (14%).11
A cadeia da sobrevivência
A ressuscitação de uma vítima adulta de parada cardíaca súbita deve seguir uma sequência ordenada, independentemente de onde o evento tenha ocorrido. Esta sequência é denominada cadeia de sobrevivência.12 Os 4 elementos que a compõem – e que devem ser instituídos o mais rápido possível – são: (1) ativação do serviço de atendimento médico de emergência; (2) início de ressuscitação cardiopulmonar (RCP) imediata e tecnicamente competente, com o mínimo possível de interrupções subsequentes na compressão torácica; (3) desfibrilação inicial; e (4) prestação de atendimento avançado.
Ativação do serviço de atendimento médico de emergência
Um indivíduo que sofre parada cardíaca é irresponsivo e não apresenta pulso palpável, embora exiba respirações agônicas que podem durar vários minutos. Confirme a irresponsividade falando alto com o paciente e sacudindo-o de leve. Se o paciente realmente estiver irresponsivo, busque socorro imediatamente chamando o serviço de atendimento médico de emergência da comunidade local (na maioria das localidades, ligando para 193). Caso o paciente já esteja no hospital, acione um código (p. ex., código azul, código 199).
Nota do editor: O código referido é o que já existe em boa parte dos hospitais brasileitos, como código azul que é a ativação de equipe específica para atendimento de parada cárdio-respiratória.
A única exceção é quando um resgatador solitário encontra uma vítima de parada não testemunhada e presumivelmente causada por asfixia. Nestes casos, o resgatador deve realizar uma RCP durante cerca de 2 minutos, antes de fazer uma pausa para acionar o serviço de emergências.13 Havendo disponibilidade de um desfibrilador externo automático (DEA), este deve ser trazido para o cenário da ressuscitação. Os DEA são fáceis de usar e podem salvar vidas.14-18
Início da ressuscitação cardiopulmonar (RCP)
Durante a espera pela chegada de um desfibrilador e de ajuda avançada, o resgatador deve avaliar as vias respiratórias do paciente, sua respiração e circulação [ver Levantamento primário, adiante], e iniciar a RCP [Tabela 1]. Quando a RCP é iniciada dentro de 4 minutos após a ocorrência do evento, a probabilidade de o paciente sobreviver é pelo menos 2 vezes maior.19,20 No decorrer de toda a ressuscitação, o fornecimento de uma RCP de qualidade, com o mínimo possível de interrupções na compressão torácica, é decisivo para a otimização da possibilidade de sobrevivência do paciente.
Tabela 1. Etapas iniciais da ressuscitação no paciente irresponsivo com idade = 8 anos
|
Confirmar a irresponsividade |
|
Acionar o sistema de emergências médicas |
|
Na maioria das comunidades, ligar 193 |
|
No hospital, acionar um “código” de resposta ( em geral código “azul”) |
|
Solicitar um DEA |
|
Iniciar o suporte vital básico (RCP) |
|
Abrir a via aérea (manter a estabilidade e o alinhamento da coluna espinal em vítimas com suspeita de traumatismo) |
|
Checar a respiração; na ausência de respiração, fornecer 2 respirações iniciais (cada uma com 1 segundo de duração, permitindo a exalação do ar entre uma e outra) |
|
Checar a pulsação carotídea (esperar < 10 segundos para avaliar); na ausência de pulsação, proceder da seguinte forma: |
|
Iniciar as compressões torácicas (“pressionar com força e rápido”) a uma frequência de 3,8 a 5,1 cm por compressão, sempre permitindo que o tórax recue totalmente entre as compressões |
|
Intercalar ventilações com compressões torácicas: em pacientes não intubados, aplicar 30 compressões, pausar por 2 respirações (isto é, um ciclo de RCP) e então repetir; em pacientes intubados, fornecer 1 respiração a cada 5 segundos, sem pausas na frequência das compressões, que deve ser de 100/min |
|
Quando o desfibrilador chegar, analisar e tratar imediatamente a arritmia; minimizar quaisquer interrupções das compressões torácicas |
|
Conectar o paciente ao DEA [Tabela 2] ou ao monitor-desfibrilador [Tabela 3] |
|
Analisar e tratar a arritmia de acordo com a necessidade [Figura 2] |
DEA = desfibrilador externo automático; RCP = ressuscitação cardiopulmonar.

Figura 2. Algoritmo de tratamento para pacientes com taquicardia ventricular (TV), fibrilação ventricular (FV), atividade elétrica sem pulsação (AESP) ou assístole.
ECG = eletrocardiograma; ET = endotraqueal; IV = via endovenosa; RCP = ressuscitação cardiopulmonar.
Tabela 2. Uso de um DEA em pacientes com idade = 8 anos
|
Chegada de um DEA (com RCP em curso) |
|
Posicionar o DEA ao lado do paciente |
|
Ligar o DEA |
|
Conectar os eletrodos ao DEA (os eletrodos talvez já estejam conectados) |
|
Prender os coxins do eletrodo no paciente (seguindo o diagrama existente nos coxins) |
|
Análises de DEA do ritmo do paciente |
|
Pausar a RCP (e garantir que ninguém esteja tocando o paciente). Pressionar o botão “Analisar” localizado no DEA (alguns dispositivos analisam o ritmo automaticamente assim que os coxins são colocados no paciente) |
|
Orientação do DEA aos resgatadores (por voz audível imediata e/ou instruções exibidas em tela) |
|
Indicação para choque: liberar o paciente (garantir que ninguém esteja tocando o paciente) e pressionar o botão “Choque” |
|
Após a aplicação do choque, finalizar imediatamente a RCP e realizar 5 ciclos (30 compressões por 2 ventilações por ciclo, em pacientes não intubados) ou cerca de 2 min de RCP em pacientes intubados; em seguida, pausar a RCP e reanalisar o ritmo. Aplicar outro choque, se o DEA assim orientar aos resgatadores. Na ausência de indicação para choque, avaliar o paciente quanto a evidências de retorno da circulação espontânea. Se tais evidências não forem encontradas, finalizar a RCP |
|
Conceito essencial: o padrão de aplicação de choque e intercalação de RCP deve ser conduzido da seguinte forma: aplicar o choque; RCP por 2 min; em seguida, reanalisar o ritmo; repetir este padrão conforme a indicação |
|
Ou |
|
Choque não indicado: reavaliar o paciente quanto à presença de sinais de circulação. Em presença destes sinais, avaliar a adequação da respiração. Na ausência de sinais de circulação, finalizar a RCP para 5 ciclos (pacientes não intubados) ou 2 min (pacientes intubados). Decorridos 2 min de RCP, reanalisar o ritmo, em seguida aplicar choque (se houver indicação) e então iniciar imediatamente as etapas de RCP, conforme já descrito. Se não houver indicação para choque, avaliar o paciente de novo em busca de sinais de circulação espontânea. Na presença destes sinais, avaliar a adequação da respiração. Caso o paciente continue sem pulso, repetir a análise do ritmo e, em seguida, iniciar as etapas de choque (se houver indicação) |
DEA = desfibrilador externo automático; RCP = ressuscitação cardiopulmonar.
Tabela 3. Uso do desfibrilador manual54,92
|
Chegada do desfibrilador (RCP em curso) |
|
Posicionar o desfibrilador ao lado do paciente |
|
Ligar o desfibrilador (o ajuste inicial do nível de energia para desfibriladores tipicamente é 200 J)* |
|
Posicionar o seletor em “Paddles ou pás”. Como alternativa, se o paciente já estiver conectado às derivações do monitor, o seletor deve ser posicionado em I, II ou III. Garantir que as 3 derivações estejam corretamente presas ao paciente e ao desfibrilador: a derivação branca no ombro direito; a derivação preta no ombro esquerdo; e a derivação vermelha nas costelas do lado esquerdo |
|
Aplicar gel nas pás do desfibrilador eletrodos ou colocar os coxins condutores sobre o tórax do paciente. Alguns dispositivos usam eletrodos adesivos descartáveis contendo gel condutor previamente aplicado. Em ambos os casos, as posições corretas das pás com o gel aplicado, coxins condutores ou paddles descartáveis são as seguintes: pá esternal no lado direito do esterno, logo abaixo da clavícula direita; pá apical no lado esquerdo da mama esquerda, centralizado junto à linha média axilar, grosso modo no 5º espaço intercostal |
|
Pausar brevemente a RCP e analisar o ritmo |
|
Se as pás forem usados para avaliar o ritmo, devem ser colocados no paciente conforme descrito, com uma compressão firme (25 lb de pressão em cada eletrodo). O ritmo então é visualmente avaliado no monitor (com o uso de derivações, avaliar o ritmo nas derivações I, II ou III). Se o ritmo estiver em TV sem pulsação ou FV, proceder do seguinte modo: |
|
Desfibrilar e finalizar imediatamente a RCP |
|
Anunciar à equipe de ressuscitação “Carregando o desfibrilador!” e pressionar o botão “Carregar” localizado nos paddles( pás) ou no desfibrilador (360 J, não sincronizado, recomendado para desfibriladores monofásicos)* |
|
Alertar a equipe de desfibrilação de que um choque de desfibrilação será descarregado: “Contarei até 3 e então descarregarei o choque! UM, eu me afasto; DOIS, vocês se afastam; TRÊS,todos se afastam!” Ao mesmo tempo em que estes alertas forem sendo feitos, deve-se garantir visualmente que nenhum membro da equipe de ressuscitação esteja em contato com o paciente |
|
Pressionar o botão “Descarga” existente em ambos as pás do desfibrilador, simultaneamente, para descarregar o choque de desfibrilação. Finalizar a RCP imediatamente após a aplicação do choque (não tentar analisar mudanças de ritmo após a aplicação do choque). Realizar 5 ciclos de RCP em pacientes não intubados (cerca de 2 min de RCP em pacientes intubados). Recarregar o desfibrilador (360 J)*, para se preparar para a etapa seguinte |
|
Pausar a RCP e reavaliar o ritmo pelo monitor. Se o paciente ainda estiver em TV ou FV, recarregar o desfibrilador (agora com 300 J)* e repetir o processo de comunicar em voz alta aos membros da equipe as 3 frases de alerta já descritas, para então aplicar o choque de desfibrilação |
|
Reavaliar o ritmo no monitor; se o paciente ainda estiver em TV ou FV, recarregar o desfibrilador (agora com 360 J)* e repetir o processo de comunicar em voz alta aos membros da equipe as 3 frases de alerta já descritas, para então aplicar o choque de desfibrilação |
|
Reavaliar o ritmo, no monitor. Se o paciente ainda estiver em TV ou FV, finalizar a RCP e continuar a sequência de ressuscitação [Figura 2] |
*Nota: Ao usar um desfibrilador bifásico, é aceitável ajustar um nível de energia desfibrilatória inicial mais baixo (< 200 J) e sem escala de energia em choques subsequentes.
FV = fibrilação ventricular; RCP = ressuscitação cardiopulmonar; TV = taquicardia ventricular.
Início da desfibrilação
Quando o DEA ou monitor-desfibrilador chega, é preciso prendê-lo corretamente ao paciente e analisar o ritmo dele. Se o paciente apresentar FV ou TV sem pulso, um choque desfibrilatório deve ser aplicado rapidamente [Tabelas 2 e 3], seguido da retomada imediata da RCP. A importância do acesso rápido à desfibrilação não pode ser superenfatizada. No caso de um paciente que esteja morrendo em decorrência de um ritmo responsivo ao choque, as chances de sobrevivência caem em 7 a 10% para cada minuto de atraso na desfibrilação.21
Início do atendimento avançado
Se o paciente permanecer sem pulso, mesmo depois que todas as etapas descritas tiverem sido seguidas, deve-se continuar a fornecer uma RCP de qualidade; deve-se estabelecer uma via aérea definitiva, certificar-se de que esta tenha sido corretamente instalada e, então fixá-la. Ao mesmo tempo, deve-se obter um acesso endovenoso (IV) e, em seguida, administrar medicações vasopressoras (adrenalina ou vasopressina) seguidas da instituição de outras intervenções apropriadas, de acordo com o ritmo e as circunstâncias da parada [ver Ressuscitação cardíaca baseada nos achados de ritmo, adiante]. Se o paciente estiver em FV ou TV sem pulsação, tentativas repetidas de desfibrilação devem ser feitas aproximadamente a cada 2 minutos, combinadas à administração de fármacos vasoativos e antiarrítmicos [Tabela 4].
Tabela 4. Fármacos úteis na parada cardíaca3,93
|
Categoria |
Fármacos e doses fornecidas |
Indicações na parada cardíaca |
Dosagem para adultos |
Comentários |
|
Vasopressores |
Adrenalina, 1 mg em seringa de emergência de 10 mL; 1 mg/mL (frascos de 1 mL e 30 mL) |
TV sem pulsação ou FV irresponsiva aos choques desfibrilatórios iniciais; AESP; assístole |
1 mg por injeção IV; pode repetir a cada 3 a 5 min, enquanto o paciente estiver sem pulso; também pode ser fornecida por via ET: 2 a 2,5 mg diluídas em SN a um volume total de 10 mL |
Os bolos IV de adrenalina (1 mg) são apropriados somente para pacientes em parada cardíaca; havendo necessidade de administração contínua de adrenalina no pós-ressuscitação, deve ser iniciada uma infusão contínua (1 a 10 mcg/min) Dose alta de adrenalina (até 0,2 mg/kg, IV, por dose) não melhora a sobrevida à alta hospitalar de pacientes em parada cardíaca e deixou de ser recomendada para adultos (exceto em casos raros, como na superdosagem de betabloqueador) |
|
Vasopressina, 20 UI/mL (frasco de 1 mL) |
Pode ser usada no lugar da 1ª e/ou 2ª dose de adrenalina, na parada cardíaca |
40 UI por injeção IV, em dose única; também pode ser fornecida por tubo ET: mesma dose, diluída em SN a um volume total de 10 mL |
Se não houver resposta após 10 min de ressuscitação contínua, administrar adrenalina subsequentemente, conforme descrito | |
|
Antiarrítmicos |
Amiodarona, 50 mg/mL (frasco de 3 mL) |
TV sem pulso ou FV irresponsiva aos choques desfibrilatórios iniciais e à administração de adrenalina (ou vasopressina) + choque(s) |
300 mg diluídas em 20 a 30 mL; injeção IV rápida de SN ou D5W; uma dose de 150 mg pode ser repetida, se houver necessidade; a dose máxima em 24 horas não deve exceder 2.200 mg |
Os possíveis efeitos colaterais são hipotensão e bradicardia, durante a fase de pós-ressuscitação |
|
Lidocaína, 50 ou 100 mg em seringas de emergência de 5 mL; bolsa pré-misturada, 1 g/250 mL ou 2 g/250 mL |
TV sem pulso ou FV irresponsiva aos choques desfibrilatórios iniciais e à administração de adrenalina (ou vasopressina) + choque(s) |
Dose inicial: 1 a 1,5 mg/kg, IV; para FV refratária ou TV instável, doses adicionais de 0,5 a 0,75 mg/kg, IV, podem ser administradas a intervalos de 5 a 10 min; dose máxima, 3 mg/kg Também pode ser administrada por via ET: 2 a 4 mg/kg diluídas em SN a um volume total de 10 mL |
Se a lidocaína for efetiva, iniciar a infusão IV contínua (2 a 4 mg/min) quando o paciente voltar a presentar um ritmo de perfusão (todavia, não usar se este for um ritmo idioventricular ou um bloqueio cardíaco de 3º grau com ritmo de escape idioventricular) A infusão contínua deve começar em 1 mg/min em casos de insuficiência cardíaca,hepatopatia crônica ou pacientes idosos | |
|
Sulfato de magnésio, 500 mg/mL (frascos de 2 mL e 10 mL), ou seringa de emergência de 10 mL |
TV sem pulso ou FV associada ao torsade de pointes, suspeita de problema de prolongamento de QT, ou outra condição de hipomagnesemia |
Administrar 1 a 2 g diluídas em 100 mL de D5W, IV, por 1 a 2 min Os déficits de magnésio corporais totais devem ser gradualmente repostos depois que a terapia inicial tiver estabilizado a emergência: administrar 0,5 a 1 g/h durante 3 a 6 horas, e então reavaliar a necessidade de continuação |
Os níveis de magnésio medidos apresentam uma correlação apenas aproximada com o nível de deficiência real Os pacientes com insuficiência renal apresentam risco de desenvolvimento de hipermagnesemia perigosa; estes casos exigem um nível apropriado de cautela Os possíveis efeitos colaterais incluem bradicardia, hipotensão, enfraquecimento generalizado e perda temporária de reflexos | |
|
Anticolinérgicos |
Atropina, 1 mg em seringa de emergência de 10 mL |
Assístolia ou AESP (se a velocidade do ritmo estiver lenta) |
Para assístolia ou AESP: 1 mg, IV, a cada 3 a 5 min até completar 3 mg Pode ser administrada via tubo ET: 2 a 3 mg diluídas em SN a um volume total de 10 mL |
A dose mínima para adultos é 0,5 mg Evitar usar em casos de bloqueio cardíaco de 2º grau de tipo II ou de bloqueio cardíaco de 3º grau |
|
Diversos |
Bicarbonato, 50 mEq em seringa de emergência de 50 mL |
Hipercalemia significativa Acidose metabólica significativa e irresponsiva a condições ideais de RCP, oxigenação e ventilação Superdosagem de certos fármacos, incluindo antidepressivos tricíclicos e aspirina |
Terapia para hipercalemia: 50 mEq, IV Acidose metabólica: 1 mEq/kg, injeção IV lenta; pode repetir metade da dose inicial em 10 min; de modo ideal, os GSA devem ajudar a guiar a terapia adicional Uso em casos de superdosagem: discutir com o toxicologista |
Em paciente hipercalêmicos não dependentes de diálise, o bicarbonato é mais útil se a acidose metabólica também estiver presente; o bicarbonato é menos efetivo em pacientes com insuficiência renal dependentes de diálise. O uso do bicarbonato no tratamento da acidose metabólica em pacientes de parada cardíaca é controverso Os possíveis efeitos colaterais podem incluir a sobrecarga de sódio, hipocalemia e alcalose metabólica |
|
Cloreto de cálcio, 100 mg/mL em seringa de 10 mL previamente preparada |
Hipercalemia significativa Superdosagem de bloqueador de canal de cálcio Hipocalcemia profunda por outras causas |
Na hipercalemia: 5 a 10 mL, injeção IV lenta; pode ser repetida, se houver necessidade Em casos de superdosagem de bloqueador de canal de cálcio: discutir com o toxicologista |
Não usar diante da suspeita de hipercalemia causada por envenenamento agudo com digoxina Não combinar com bicarbonato de sódio na mesma injeção IV O cloreto de cálcio não é uma medicação de rotina na parada cardíaca |
Nota: Todas as medicações usadas durante uma parada cardíaca, quando administradas através de um sítio venoso periférico em um membro, devem ser seguidas do fornecimento de um bolo de salina de 20 mL por via IV e elevação do membro por 10 a 20 segundos.
AESP = atividade elétrica sem pulso; D5W = dextrose a 5% em água; ET = endotraqueal; FV = fibrilação ventricular; GSA = gases no sangue arterial; RCP = ressuscitação cardiopulmonar; SN = salina normal; TV = taquicardia ventricular.
Resultado da ressuscitação
Quando cada elo da cadeia de sobrevivência é rápido e sequencialmente disponibilizado, o paciente tem a oportunidade ideal de recuperar a circulação espontânea.21-24 Nos Estados Unidos, comunidades individuais relatam taxas de sobrevida de 4 a 40% ou mais em casos de morte súbita cardíaca.25-29 As vítimas pré-hospitalares de FV têm apresentado taxas de sobrevida à alta hospitalar acima de 50%, quando um DEA é empregado ativamente.30 Todavia, existem numerosos fatores diferentes que também influenciam a sobrevida do paciente. Entre estes fatores, estão o fato de o evento sofrido pelo paciente ter sido testemunhado; a rapidez e efetividade da RCP no local do evento; o número e a duração das interrupções à RCP; o ritmo associado à parada cardíaca; e as comorbidades subjacentes.31,32 No caso de uma parada cardíaca intra-hospitalar, por exemplo, as taxas de sobrevida gerais variam de 9 a 32%.32-39 Em um estudo, a sobrevivência até a alta hospitalar foi de 30% para os pacientes com cardiopatia primária; 15% para pacientes com doenças infecciosas; e apenas de 8% para os pacientes que apresentavam outras doenças em estágio terminal (p. ex., câncer, doença pulmonar, insuficiência hepática ou insuficiência renal).40
Estas estatísticas destacam a importância do uso apropriado e discriminado da ressuscitação cardíaca. A ressuscitação cardíaca fornecida pelos resgatadores, com auxílio de ferramentas poderosas, salva as vidas de milhares de pessoas a cada ano. Essas técnicas conseguem resgatar os pacientes que, de outro modo, perderiam uma vida produtiva e significativa. No entanto, a ressuscitação cardíaca não deve ser empregada para reverter a morte que chega no tempo devido nem a morte natural. Em tais circunstâncias, a ressuscitação cardíaca tem o potencial de prolongar o processo de morte e aumentar o sofrimento humano. Todos os profissionais são devidamente orientados a lembrar que “a morte não é o oposto da vida, e sim do nascimento, e ambos são aspectos da vida.”41 É a morte prematura que requer intervenção com ressuscitação cardíaca.
Levantamentos primário e secundário de ressuscitação cardíaca
Uma ressuscitação cardíaca é um evento estressante para todos os envolvidos. Com muita frequência, as paradas cardíacas que ocorrem em clínicas e hospitais, bem como seu manejo, são episódios caóticos nas ocupadas vidas dos residentes e médicos atendentes. Mesmo assim, estabeleceu-se de maneira eloquente que uma equipe de ressuscitação eficiente deve atuar como se fosse uma sinfonia ou orquestra finamente ajustada.42 Estes níveis de habilidade exigem dedicação, tanto na prática individual como em equipe, além de uma cuidadosa organização em equipe. A maestria na realização da ressuscitação cardíaca, de fato, é algo que se persegue pela vida e requer treinamento e retreinamento em suporte cardíaco vital avançado (ACLS, advanced cardiac life support); prática e revisão regular; além de desenvolvimento de habilidades de liderança e trabalho em equipe. Seus elementos-chave incluem não só a ressuscitação em si, mas também a resposta ao anúncio do evento ( equipes de código azul), estabilização do paciente no pós-ressuscitação, notificação da família e prestador de assistência primária, códigos críticos e prestação de contas. Para ajudar os profissionais a aprenderem e colocarem em prática algumas das técnicas mais essenciais empregadas na ressuscitação cardíaca de modo mais simples e efetivo, a American Heart Association (AHA) desenvolveu os conceitos de atendimentos primário e secundário de um paciente em parada cardíaca atraumática.43
O levantamento primário
O atendimento primário de uma vítima de parada cardíaca súbita consiste em uma avaliação apropriada das (A) vias respiratórias do paciente (airway), (B) respiração (breathing) e (C) circulação, bem como na aplicação de uma RCP especializada até que seja possível realizar a (D) desfibrilação (considerando que o paciente esteja em FV ou TV sem pulsação). Assim, o levantamento primário inclui o 2º e 3º elos da cadeia de sobrevivência (ver anteriormente).
Em 1958, Kouwenhoven observou que quando seus colegas de pesquisa forçosamente aplicavam eletrodos de desfibrilação externos no tórax de um cachorro, no laboratório, ocorria uma onda de pressão arterial.44 Estudos e refinamentos adicionais conduziram à técnica de RCP torácica-fechada, cuja descrição detalhada foi publicada em 1960.45 O 1º relato do uso desta técnica em pacientes data de 1961.46 Desde então, os fundamentos da RCP torácica-fechada permaneceram relativamente inalterados. A ventilação boca-a-boca, boca-máscara ou balão-válvula-máscara oxigena o sangue. As compressões torácicas produzem um fluxo sanguíneo que segue para a frente. Este fluxo parece resultar de uma combinação da compressão direta do coração e das alterações da pressão intratorácica com a compressão torácica e subsequente recuo do tórax.47,48
A RCP isolada não promove a desfibrilação do coração. Seu principal benefício consiste em estender a viabilidade do paciente até a disponibilização de um desfibrilador e de uma intervenção avançada e, espera-se, a restauração bem-sucedida da circulação espontânea do paciente. A RCP não é tão efetiva quanto a contração cardíaca. Picos de pressão arterial sistólica da ordem de 60 a 80 mmHg podem ser gerados, contudo a pressão arterial diastólica permanece baixa. Além disso, mesmo sob condições ideais, somente pode ser alcançado um débito cardíaco equivalente a 25 a 30% do normal.49 Mesmo assim, uma RCP efetiva é essencial para manter o paciente vivo. É preciso lembrar que os resgatadores mais importantes atuantes na ressuscitação cardíaca são em geral aqueles que executam RCP especializada, pois é somente graças aos esforços destes profissionais que o coração e o cérebro dos pacientes permanecem viáveis até que a desfibrilação e outras intervenções avançadas consigam restaurar a circulação espontânea. Uma RCP de qualidade, incluindo a aplicação especializada de compressões torácicas, deve ser realizada com o mínimo possível de interrupções no decorrer da tentativa de ressuscitação.
Após a confirmação da irresponsividade, então o serviço de atendimento médico de emergência é ativado e um DEA é solicitado. O atendimento primário (A, B, C e D) deve ser realizado conforme descrito (ver adiante), até a chegada do DEA.
Nota do editor. As alterações mais recentes do ACLS privilegiam iniciar imediatamente apos pedido de ajuda das compressões torácicas, o que torna na verdade o item C o primeiro da cadeia.
Otimização das vias aéreas
Abre-se a boca do paciente e otimizam-se as vias aéreas dele empregando a manobra inclinação da cabeça e elevação do queixo. Se houver suspeita de lesão espinal, deve-se usar a manobra do empurrão mandibular, em vez da técnica de inclinação da cabeça. Em pacientes com suspeita de lesão espinal, o alinhamento correto da coluna espinal deve ser mantido ao longo de todas as fases da ressuscitação. Nestas circunstâncias, enquanto os equipamentos vão sendo disponibilizados, a coluna espinal do paciente exige imobilização com tábua acolchoada, colar cervical rígido e suporte apropriado ao redor da cabeça do paciente (para evitar a movimentação). Além disso, o paciente deve ser preso com correias à tábua imobilizadora.50
Avaliação da respiração
Para avaliar a respiração, o resgatador aproxima a própria face da boca do paciente e olha, escuta e sente as respirações deste. Se as respirações foram agônicas ou o paciente estiver apneico, o resgatador então aplica 2 respirações iniciais. Cada respiração é fornecida ao longo de 1 segundo. O tórax do paciente deve subir a cada respiração fornecida, e a expiração deve ser permitida entre as respirações. As respirações podem ser fornecidas utilizando-se a técnica de boca-a-boca aliada às devidas precações de barreira (o nariz do paciente deve ser pinçado, quando esta técnica é adotada), ou por meio da técnica de boca-máscara. O dispositivo ideal, quando disponível, consiste em um balão-válvula-máscara acoplado a um alto fluxo de oxigênio. Este dispositivo possibilita o fornecimento de uma concentração de oxigênio substancialmente maior ao paciente. Se não for possível ventilar o paciente, o resgatador deve reposicionar as vias aéreas e tentar executar a técnica novamente. Caso as vias aéreas permaneçam obstruídas, então devem ser aplicados até 5 compressões abdominais, seguidos da observação da boca para detecção de algum corpo estranho (varrer a orofaringe com o dedo, se for detectado um corpo estranho). Feito isto, repetem-se as tentativas de ventilação. A intervenção definitiva para um caso de obstrução de vias aéreas no contexto hospitalar pode envolver a visualização laringoscópica da causa da obstrução e a remoção do corpo estranho. Diante da impossibilidade de se estabelecer uma via aérea adequada por métodos menos invasivos, talvez seja necessário realizar uma cricotireotomia.
Nota do editor: Como já pontuado atualmente se privilegia apos a constatação de PCR e abertura das vias aéreas a realização de compressões torácicas e nao de respirações.
Início da ressuscitação cardiopulmonar (RCP)
Em seguida, o resgatador do atendimento médico deve checar o pulso na carótida do paciente irresponsivo, e este procedimento não deve durar mais do que 10 segundos. (A AHA não mais recomenda a realização de checagens de pulsação por resgatadores que não sejam profissionais da saúde.51 Em vez disso, os resgatadores leigos devem iniciar as compressões torácicas se o paciente não respirar, tossir nem se mover após a aplicação das 2 respirações iniciais.) Se o paciente estiver sem pulsação na carótida, as compressões torácicas devem ser iniciadas. O paciente deve estar sobre uma superfície firme, e a região carpal da mão do resgatador deve estar posicionada no centro da metade inferior do esterno do paciente (e voltada na direção craniana em relação ao processo xifoide), mais ou menos ao nível dos mamilos. A outra mão do resgatador deve ser posicionada por cima da outra, com os dedos de ambas entrelaçados.
Os braços do resgatador devem permanecer retos, e a força de cada compressão deve vir de seu tronco. Em pacientes com idade igual ou superior a 8 anos, o esterno é firmemente comprimido em 3,8 a 5,1 cm e, então, liberado. A frequência de compressões torácicas recomendadas é de 100/minuto para pacientes com idade igual ou superior a 8 anos. É preciso permitir que o tórax retorne às dimensões pré-compressão entre as compressões, porém a região carpal da mão do resgatador que estiver mais próxima do paciente deve permanecer em contato com o esterno dele.
Em pacientes não intubados, as compressões torácicas são brevemente pausadas para o fornecimento das ventilações. A sequência é a mesma, independentemente de haver 1 ou 2 resgatadores realizando a RCP: um resgatador aplica 30 compressões, faz uma pausa de 2 respirações (cada uma com duração de 1 segundo) e, em seguida, finaliza as compressões. Uma sequência de 30 compressões e 2 respirações é denominada um ciclo de RCP. Em pacientes com tubo endotraqueal (ET), não é necessário fazer pausas para ventilação. Em vez disso, a cada 5 segundos, uma ventilação é fornecida por 1 segundo, enquanto as compressões são mantidas a uma frequência de 100/minuto.20
As condições ideais de RCP, em termos de momento e proporção ventilação:compressões, atualmente são uma área de pesquisa. Os estudos já realizados nesta área levaram à modificação da antiga proporção de 15 compressões a cada 2 ventilações para a proporção recomendada em 2005, de 30 compressões a cada 2 ventilações.52 Em um modelo suíno, por exemplo, o resultado neurológico ideal foi alcançado com a aplicação apenas de compressões torácicas durante os primeiros 4 minutos, seguidas da aplicação de compressões e ventilações a uma proporção compressão:ventilação de 100:2.53 No contexto pré-hospitalar, havendo disponibilidade de assistência rápida e avançada em questão de minutos, o fornecimento de ventilação boca-a-boca bystander-iniciada aliado à aplicação de compressões torácicas não proporciona nenhuma vantagem em relação ao uso isolado das compressões torácicas.54
O uso de uma técnica eficiente é decisivo ao longo de todo o processo de fornecimento da RCP. O paciente deve apresentar pulsações carotídeas com a aplicação das compressões torácicas, bem como apresentar sons respiratórios apropriados e movimento torácico com o fornecimento das ventilações. Notavelmente, as pulsações femorais observadas com a RCP não necessariamente indicam uma RCP efetiva. Estas pulsações muitas vezes são venosas, e não arteriais. As medidas quantitativas dos níveis de dióxido de carbono ao final de uma expiração normal podem ser monitoradas, desde que praticáveis. Níveis altos estão correlacionados com uma RCP mais efetiva e uma sobrevida aumentada55 [Tabela 1].
Nota do editor: Apesar de o texto algumas vezes colocar como tempo máximo de checagem de pulso como 10 segundos, a recomendação é que este procedimento nao leve mais que 5 segundos.
Desfibrilação
Quando o monitor-desfibrilador ou o DEA chegam, devem ser instalados no paciente. O ritmo é analisado e, se o paciente estiver em FV ou TV sem pulsação, deve ser realizada a desfibrilação [Tabelas 2 e 3]. A RCP deve ser iniciada imediatamente. Os resgatadores devem continuar determinando os efeitos da desfibrilação até que 5 ciclos de RCP tenham sido concluídos. Mais uma vez, a meta consiste em maximizar as compressões torácicas e minimizar as interrupções durante a execução da RCP. Após 5 ciclos, reavalia-se o ritmo e, se um ritmo de perfusão em potencial aparentemente estiver presente, avalia-se a pulsação carotídea.
Acredita-se que a desfibrilação atue despolarizando simultaneamente uma massa de miócitos cardíacos suficiente para tornar o tecido cardíaco à frente das ondas frontais de TV ou FV refratário à condução elétrica. Subsequentemente, o nodo sinusal ou outra região marca-passo cardíaca apropriada com automaticidade inerente podem finalizar a despolarização-repolarização ordenada, com consequente retorno a um ritmo de perfusão.17,56 Quanto mais cedo a desfibrilação ocorrer, maior será a probabilidade de ressuscitação. A desfibrilação fornecida imediatamente após o início da FV está associada a um índice de sucesso altíssimo.57 Em um estudo sobre pacientes que sofreram parada cardíaca súbita enquanto jogavam nos cassinos de Nevada (Estados Unidos), a taxa de sobrevivência até a alta hospitalar foi de 74% para os pacientes que receberam a 1ª desfibrilação dentro de um período de 3 minutos após sofrerem um colapso testemunhado.30 Neste estudo, a desfibrilação foi fornecida por um DEA operado pelos seguranças do cassino.
A desfibrilação inicial é tão decisiva que, se um desfibrilador for disponibilizado imediatamente, seu uso tradicionalmente precede a RCP em casos de pacientes em FV ou TV sem pulsação de início testemunhado. Se a RCP já estiver em andamento, com certeza deve ser brevemente interrompida para que a desfibrilação seja realizada.
Os desfibriladores mais modernos podem compensar a impedância torácica, garantindo que o nível de energia selecionado seja de fato a energia fornecida ao tecido miocárdico. Além disso, os desfibriladores que realizam uma desfibrilação bifásica em ondas, em vez da desfibrilação monofásica em ondas sinusoidais lentas padrão, proporcionam uma desfibrilação efetiva a níveis energéticos mais baixos (< 200 J) e dispensam a escalada do nível de energia em choques subsequentes.17,58-61 No estudo Optimized Response to Cardiac Arrest (ORCA), que envolveu 115 pacientes em FV pré-hospitalar, um DEA com choque bifásico de 150 J foi mais efetivo do que um DEA de choque monofásico de alta energia tradicional em relação a 4 aspectos: (1) obteve maior sucesso na produção de desfibrilação com o 1º choque (96% vs. 59%); (2) levou a um maior índice de sucesso final com a desfibrilação (100% vs. 84%); (3) promoveu uma maior taxa de retorno da circulação espontânea (76% vs. 54%); e (4) seu uso estava associado a um maior índice de bom desempenho cerebral entre os sobreviventes (87% vs. 53%).62 Contudo, ambos os desfibriladores não diferiram quanto à sobrevida até a admissão ou alta hospitalar e, até hoje, não há nenhuma réplica sobre os achados do ORCA. Segundo as atuais diretrizes da AHA, os desfibriladores bifásicos em ondas de baixa energia são seguros e apresentam eficácia equivalente ou maior na eliminação da FV, em comparação aos desfibriladores monofásicos em ondas padrão.17,52
As pesquisas em curso sugerem que a duração da FV deve ser considerada ao se decidir se a desfibrilação deve ser feita imediatamente e tão logo um desfibrilador seja disponibilizado ou se uma RCP de curta duração deve ser fornecida primeiro, para “condicionamento cardíaco”, antes de se proceder à desfibrilação. No modelo suíno, em um contexto de FV prolongada (> 10 min), o fornecimento de RCP antes do contrachoque proporcionou vários benefícios fisiológicos.63 Estudos demonstraram que os pacientes em FV com duração acima de 5 minutos apresentaram retorno da circulação espontânea mais satisfatório, maior sobrevida à alta hospitalar e maior sobrevida de 1 ano nos casos em que a equipe da ambulância forneceu 3 minutos de RCP antes de realizar a desfibrilação, do que quando a desfibrilação foi realizada pela equipe da ambulância imediatamente após a chegada na cena. Entretanto, alguns especialistas questionam a validade destes resultados, com base no delineamento do estudo.64,65 Segundo as diretrizes de 2005, o fornecimento de RCP por cerca de 5 ciclos antes de buscar socorro é recomendado para os casos em que o resgatador está sozinho e a vítima sofreu uma parada cardíaca não testemunhada e presumivelmente por asfixia (p. ex., por quase-afogamento).64,65
O atendimento secundário
O atendimento secundário para uma vítima de parada cardíaca persistente é realizado após a conclusão do atendimento primário. De novo, é fundamental fornecer uma RCP com o mínimo possível de interrupções das compressões torácicas durante todo o processo. Assim como no atendimento primário, o atendimento secundário segue um formato ABCD, que, neste caso, consiste em intervenções avançadas (A) nas vias respiratórias; otimização da ventilação e oxigenação por meio da confirmação da colocação do tubo ET e avaliação repetida da adequação das respirações (breaths) (B) fornecidas; acesso IV e administração de medicação apropriada para a circulação (C) do paciente; e terapia definitiva (D), determinada com base em um diagnóstico diferencial que considere os processos patológicos específicos tidos como responsáveis (ou contribuintes) para a parada cardíaca. O levantamento secundário inclui o 4º elo da cadeia de sobrevivência – o atendimento avançado rápido (ver anteriormente).
Colocação de vias aéreas avançadas
Os pacientes que permanecem em parada cardíaca após a conclusão do levantamento primário requerem a colocação de uma via respiratória avançada. Dependendo do contexto e da experiência dos resgatadores, esta via respiratória pode ser uma máscara respiratória laríngea, um Combitube (um tubo traqueal conectado de lado a lado a um obturador) esôfago-traqueal ou um tubo ET.38,66,67 A máscara respiratória laríngea e o Combitube podem ser colocados por uma equipe menos treinada do que aquela necessária à colocação de um tubo ET. Além disso, dispensam equipamentos adicionais e visualização das cordas vocais. Mesmo assim, a intubação ET oral geralmente é a técnica de via respiratória avançada preferida para as ressuscitações cardíacas em curso, em especial no cenário hospitalar, onde costuma haver intubadores experientes. No contexto pré-hospitalar, as evidências que sustentam a intubação ET ainda são inconsistentes. A intubação ET isola a via aérea, mantém a patência da via respiratória, ajuda a proteger a traqueia contra o risco permanentemente presente de aspiração, ajuda a possibilitar a oxigenação e ventilação ideais do paciente, permite a sucção traqueal e até fornece uma via de distribuição de algumas medicações para a circulação sistêmica (via circulação pulmonar) nos casos em que o acesso venoso é inviável ou foi perdido.66
Otimização da respiração e da ventilação
Quando um paciente em parada cardíaca é submetido à intubação ET, o posicionamento correto do tubo ET deve ser confirmado imediatamente e, durante e após a ressuscitação, a intervalos regulares [Tabela 5]. Recomenda-se o uso rotineiro de um dispositivo detector esofágico ou detector de CO2 no final da expiração, bem como o exame detalhado do paciente. É preciso ter cautela ao usar os detectores de CO2 colorimétricos qualitativos, pois há relatos de resultados falso-positivos e falso-negativos obtidos durante a parada cardíaca.68 Os sons respiratórios devem estar presentes à auscultação sobre as paredes torácicas anterior e lateral, assim como o tórax do paciente deve subir e descer com o fornecimento das ventilações. À ausculta do epigástrio, nenhum murmúrio deve ser ouvido. O tubo ET deve ser inserido até a marca de profundidade correta para um indivíduo adulto de tamanho mediano, ou seja, 21 cm adentro pelo canto da boca de uma mulher e 23 cm adentro pelo canto da boca de um homem. A cor da pele do paciente deve estar razoável (isto é, nem escurecida, nem cianótica), desde que sua pigmentação permita realizar este tipo de avaliação.
Uma vez confirmado o posicionamento correto, o tubo ET então é devidamente fixado para evitar seu deslocamento. Quando for viável, a medida de gasometria no sangue arterial (GSA) será útil para fornecer confirmação adicional da adequação da oxigenação e da ventilação enquanto a ressuscitação estiver em curso.
Tabela 5. Confirmação da colocação do tubo ET
|
Processo de intubação |
|
As cordas vocais são visualizadas pelo intubador |
|
A ponta do tubo ET pode ser vista passando entre as cordas vocais |
|
O manguito do tubo ET também está passando entre as cordas vocais, a uma distância de 1 cm |
|
Checagens pós-intubação |
|
O dispositivo detector esofagiano ou o detector de CO2 confirmam a colocação do tubo ET na traqueia |
|
Os sons respiratórios são simétricos (auscultar sobre a região torácica anterior lateral e junto à linha média axilar, bilateralmente) |
|
Nenhum murmúrio é ouvido à auscultação sobre o epigástrio |
|
O tórax do paciente sobe e abaixa corretamente em resposta à ventilação |
|
A profundidade do tubo ET é adequada: 21 cm adentro pelo canto da boca em mulheres, e 23 cm adentro pelo canto da boca em homens |
|
Fixar o tubo ET para evitar seu deslocamento |
|
Reavaliar a adequação da oxigenação e ventilação ao longo de toda a ressuscitação (avaliação de cabeceira do paciente; obter também a medida dos GSA, quando possível) |
|
Pós-ressuscitação; obter uma radiografia torácica portátil |
ET = endotraqueal; GSA = gases no sangue arterial.
Estabelecimento do acesso circulatório
O acesso à circulação venosa do paciente é obrigatório. Este tipo de acesso pode ser obtido por um ou mais membros da equipe de atendimento ao mesmo tempo, enquanto os demais ressuscitadores prosseguem com as etapas A e B do levantamento secundário. De modo ideal, uma grande cânula IV é inserida em uma veia proeminente de membro inferior ou na veia jugular externa, com o intuito de otimizar a administração das medicações necessárias. Diante da inacessibilidade de uma linha periférica, as demais possibilidades de acesso adicionais incluem a colocação de uma linha central através da veia jugular interna, veia subclávia (via abordagem supraclavicular) ou, de modo menos ideal, veia femoral. Até mesmo o acesso intraósseo é possível (a via intraóssea costuma ser utilizada para acesso vascular em emergências pediátricas, mas é pouco usada como via de acesso em pacientes adultos). É útil lembrar, como já observado, que algumas medicações de ressuscitação importantes podem ser administradas via tubos ET em casos de falha do acesso IV. Entre estas medicações, estão a naloxona, atropina, vasopressina, adrenalina e lidocaína (mnemônica: NAVEL).
As medicações comumente utilizadas na ressuscitação cardíaca podem ser agrupadas nas seguintes categorias gerais: vasopressores (adrenalina ou vasopressina); antiarrítmicos (amiodarona, lidocaína e magnésio); agentes anticolinérgicos (atropina, se a arritmia da parada for assistólica ou a AESP for lenta); e fármacos diversos utilizados no tratamento de problemas específicos que contribuem para a condição de parada, tais como bicarbonato de sódio (para casos de acidose metabólica severa, hipercalemia e superdosagem de certos fármacos) e cloreto de cálcio (para hipercalemia, superdosagem de fármaco bloqueador de canal de cálcio, ou hipocalcemia severa) [Tabela 4]. O agente antiarrítmico procainamida atualmente não é recomendado para uso em casos de parada cardíaca.
Indivíduos em parada cardíaca (que pode resultar de uma TV sem pulsação, FV, AESP ou assístole) necessitam de um vasopressor pelo tempo que permanecerem sem pulsação. Esta medicação tipicamente consiste na administração de 1 mg de adrenalina IV, a cada 3 a 5 minutos. A adrenalina estimula os receptores adrenérgicos, com consequente vasoconstrição e otimização do fluxo sanguíneo gerado pela RCP para o coração e cérebro. A vasopressina (40 UI, IV, 1 vez/dia) constitui uma alternativa razoável à adrenalina, pelo menos inicialmente. A vasopressina, usada na dose recomendada, é um potente vasoconstritor. Além disso, em relação à adrenalina, a vasopressina teoricamente proporciona a vantagem de não aumentar o consumo miocárdico de oxigênio nem a produção de lactato no coração em parada.69 Apesar de suas potenciais vantagens, em um estudo envolvendo 200 pacientes internados com parada cardíaca, a vasopressina não produziu uma taxa de sobrevida melhor do que aquela promovida pela adrenalina.70 A vasopressina mostrou-se comparável à adrenalina no tratamento de pacientes em parada cardíaca fora do hospital, quando o ritmo estava em FV ou AESP, mas foi superior à adrenalina no tratamento de pacientes em assístolia.71,72
Durante a ressuscitação com a RCP em curso, a administração da medicação através de uma cânula IV precisa ser seguida da administração de um bolo de 20 mL de salina. Se a cânula estiver inserida em uma veia periférica, o membro que a contém deve permanecer elevado durante 10 a 15 segundos, a fim de intensificar a distribuição da medicação para a circulação central. Isto é especialmente importante, devido à condição de baixo fluxo circulatório com a RCP torácica fechada.
Diagnóstico diferencial e tratamento definitivo
A parte mais desafiadora do atendimento secundário, bem como do manejo de ressuscitação cardíaca em geral, consiste na resolução de problemas que se faz necessária quando a circulação espontânea não retorna mesmo após a instituição das intervenções iniciais apropriadas. Esta situação impõe uma questão decisiva aos ressuscitadores: por que este paciente está morrendo bem agora? O desafio intelectual desta questão, que os ressuscitadores devem diligentemente tentar responder e à beira do leito, é acrescido da intensidade emocional que permeia a maioria das ressuscitações cardíacas.
Os problemas solucionáveis que podem interferir na ressuscitação podem ser agrupados em 3 categorias amplas: técnica [Tabela 6], fisiológica e anatômica [Tabela 7]. Os problemas técnicos consistem nas dificuldades relacionadas com os equipamentos ou habilidades dos ressuscitadores. Estas dificuldades incluem a RCP inefetiva; a ocorrência de muitas interrupções durante a RCP; oxigenação e ventilação inadequadas; complicações associadas ao tubo ET; dificuldades de acesso IV; e defeito de funcionamento ou uso incorreto do monitor-desfibrilador. Os problemas fisiológicos e anatômicos consistem nas condições prejudiciais à vida, embora potencialmente tratáveis, que podem ter levado à parada cardíaca em 1º lugar. Esta diferenciação entre fisiologia e anatomia é admitidamente artificial, uma vez que a fisiologia sempre está envolvida na parada cardíaca. Entretanto, esta diferenciação tem alguma utilidade como ferramenta de ensino e solução de problemas. Os problemas fisiológicos classicamente incluem a hipóxia, acidose, hipercalemia, hipocalemia severa, hipotermia, hipoglicemia e superdosagem farmacológica. Os problemas anatômicos são a hipovolemia/hemorragia, pneumotórax por tensão, tamponamento cardíaco, infarto do miocárdio e embolia pulmonar.43
Sempre que possível, a história médica e cirúrgica do paciente, além das circunstâncias e sintomas imediatamente anteriores à parada cardíaca devem ser investigados junto a seus familiares, observadores do episódio ou equipe de funcionários do hospital, durante o prosseguimento da ressuscitação. Esta informação pode conter indícios importantes sobre o principal problema causador da parada cardíaca e sobre o grau de diligência por ventura requerido para tratá-lo. Exemplificando, um paciente que chega ao departamento de emergência com dor torácica e então sofre uma parada cardíaca em FV muito provavelmente está sofrendo um infarto do miocárdio em massa, embolia pulmonar ou dissecação aórtica, bem como pneumotórax por tensão ou tamponamento cardíaco.
As questões específicas a serem consideradas incluem as seguintes: O paciente possui fatores de risco de cardiopatia, embolia pulmonar ou doença aórtica? Qual era a qualidade da dor do paciente e da irradiação dessa dor antes da parada cardíaca? Como estavam os sinais vitais e quais eram os achados do exame físico pré-parada? O que o eletrocardiograma (ECG) pré-parada mostrou (se estiver disponível)? É possível usar quaisquer uma destas informações agora, à beira do leito, para estabelecer a necessidade de intervenções de ressuscitação durante a fase D do levantamento secundário? Exemplificando, se o ECG pré-parada mostrou uma elevação proeminente do segmento ST nas derivações V1 a V4, que seja consistente com um extenso infarto do miocárdio anterior; se a ressuscitação do paciente estiver falhando mesmo com a instituição das intervenções apropriadas; e se aparentemente não houver problemas técnicos que impeçam a ressuscitação – então é possível estabelecer um diagnóstico funcional de infarto do miocárdio maciço. Neste caso, a terapia trombolítica IV pode ser uma etapa razoável e necessária deste processo de ressuscitação.73
Uma cuidadosa consideração das possíveis razões por trás da falha de uma ressuscitação em geral levam ao limite a experiência e as habilidades clínicas da equipe de ressuscitação e do líder da equipe codificada. Mesmo assim, a falha em considerar estes aspectos formidáveis deprivam o paciente de uma ótima oportunidade de sobreviver à parada cardíaca.
Tabela 6. Problemas técnicos que podem impedir o sucesso da ressuscitação
|
Problema |
Pacientes de risco |
Recomendações |
|
RCP inefetiva |
Todos os pacientes em parada cardíaca |
Minimizar as interrupções durante as compressões torácicas Garantir uma RCP tecnicamente perfeita Confirmar as pulsações carotídeas com a RCP (“pressionar com força e rápido”) Se a linha arterial tiver sido colocada antes da parada cardíaca, confirmar a adequação da ondulação arterial com a RCP, no monitor da linha arterial Monitorar o CO2 expiratório ( EtCO2) , quando disponível (níveis aumentados estão correlacionados a uma RCP mais eficiente e à melhora da sobrevida do paciente) Confirmar a adequação da oxigenação por Gasometria arterial, quando viável |
|
Oxigenação e ventilação inadequadas |
Todos os pacientes em parada cardíaca |
Garantir o posicionamento e controle ideais da via respiratória Contar com a disponibilização imediata da sucção, para manejar as secreções faríngeas e das vias aéreas Garantir o uso de uma máscara facial firmemente vedada e com ajuste adequado, para fornecimento de ventilação com máscara balão-válvula (MBV) até o estabelecimento de uma via aérea definitiva Para os pacientes não intubados, a sequência é de 30 compressões:2 ventilações seguidas de repetição Aplicar pressão cricoide para prevenir a distensão gástrica durante a ventilação MBV, até o estabelecimento de uma via aérea definitiva Garantir que o oxigênio suplementar esteja fluindo para a MBV a uma velocidade de 15 L/min Fornecer um volume corrente apropriado por ventilação (6 a 7 mL/kg, se houver oxigênio disponível), a uma frequência de 12 a 15 respirações/min Confirmar a presença de sons respiratórios bilaterais e iguais acompanhando a ventilação Confirmar a subida do tórax do paciente a cada ventilação Dar tempo suficiente para a exalação do ar entre as respirações Confirmar a condições ideais de oxigenação e ventilação por medida de GSA, quando viável |
|
Dificuldades associadas ao tubo ET |
Todos os pacientes com tubo ET |
Aguardar = 20 a 30 segundos/tentativa de intubação O intubador deve ver a ponta do tubo ET e o manguito do tubo passando entre as cordas vocais no momento da intubação Após a intubação, confirmar imediatamente a correta colocação do tubo ET [Tabela 5]; a intervalos regulares, reconfirmar a posição do tubo ET ao longo de toda a ressuscitação Confirmar a condições ideais de oxigenação e ventilação pela medida gasométrica. Após a intubação, considerar a colocação do tubo nasogástrico para descomprimir o estômago e otimizar as excursões diafragmáticas com a ventilação |
|
Dificuldades associadas à linha IV |
Todos os pacientes em parada cardíaca |
Colocar pelo menos uma cânula IV de calibre 18 em um sítio da veia jugular externa ou da veia antecubital Checar regularmente a existência de acesso IV, no decorrer de toda a ressuscitação Após a administração de todas as medicações através de um acesso IV periférico, fornecer um bolo de 20 mL de salina e manter o membro que contém a linha IV elevado por 10 a 15 segundos (quando possível) Considerar a instalação de um acesso venoso central, se a ressuscitação for prolongada Estar atento a cada infusão IV fornecida ao paciente Suspender todas as medicações não essenciais iniciadas antes da parada cardíaca (p. ex., nitroglicerina) Durante a ressuscitação, as únicas infusões que o paciente deve receber são de salina normal, produtos do sangue (quando houver indicação clínica) e medicações pertinentes necessárias para auxiliar o retorno da circulação espontânea Os cateteres arteriais pulmonares e as acesso venosos centrais ocasionalmente atuam como focos arritmogênicos junto ao ventrículo direito. Quando aplicável, desinflar todos os balões relevantes conectados ao cateter e removê-lo para uma posição junto à veia cava superior |
|
Dificuldades associadas ao monitor-desfibrilador |
Todos os pacientes em parada cardíaca |
Certificar-se de que o botão de “Modo Sincronizado” esteja desligado durante a desfibrilação de pacientes em FV ou TV sem pulsação Garantir que a eletricidade não forme um arco sobre o tórax do paciente, devido à transpiração ou ao gel condutor espalhado sobre a área; secar o tórax do paciente com uma toalha, exceto nas áreas localizadas diretamente embaixo dos coxins ou pás. Não aplicar choque através de adesivos ou pastas de nitroglicerina Se o paciente tiver um CDI ou um marca-passo, ainda sim pode ser desfibrilado manualmente, mas o choque não deve ser aplicado diretamente sobre o dispositivo interno; nestas circunstâncias, os coxins ou pás devem ser colocados a uma distância mínima de 2,5 cm em relação ao dispositivo interno do paciente; se o CDI estiver emitindo disparos intermitentes e não estiver desfibrilando o paciente, e se for considerado que o CDI está comprometendo a ressuscitação, o dispositivo deve ser desligado com um ímã para que a desfibrilação manual possa ocorrer sem nenhuma interferência Maximizar o ganho ou “tamanho” da análise de ECG e checar o ritmo em várias derivações (ou mudar os eixos das pás , ao fazer a leitura no modo “Paddle ou pás”), a fim de confirmar a assístolia, quando o ritmo inicial parecer estar em assístolia. |
CDI = cardioversor-desfibrilador interno; ECG = eletrocardiograma; ET = endotraqueal; FV = fibrilação ventricular; GSA = gases no sangue arterial; IV = endovenosa; RCP = ressuscitação cardiopulmonar; TV = taquicardia ventricular.
Tabela 7. Condições potencialmente tratáveis que podem causar ou contribuir para a parada cardíaca3
|
Condição |
Contexto clínico |
Diagnóstico e ações corretivas |
|
Acidose |
Acidose preexistente, diabetes, diarreia, fármacos, toxinas, ressuscitação prolongada, doença renal, choque |
Obter a medida imediata de gasometria arterial( GSA). Reavaliar a qualidade técnica da RCP, oxigenação e ventilação Confirmar a correta colocação do tubo ET Hiperventilar o paciente (PaCO2 de 30 a 35 mmHg) para compensar parcialmente a acidose metabólica Se o pH < 7,2 mesmo após a instituição das intervenções descritas, considerar a administração IV de bicarbonato de sódio (injeção IV lenta de 1 mEq/kg ) |
|
Tamponamento cardíaco |
Diátese hemorrágica, malignidade, pericardite, cirurgia pós-cardíaca, infarto pós-miocárdio, traumatismo |
Iniciar a ressuscitação com grandes volumes de cristaloide por via IV Confirmar o diagnóstico com um ecocardiograma de cabeceira emergencial, quando disponível Realizar pericardiocentese A intervenção cirúrgica imediata é apropriada, se a pericardiocentese for inútil, mas houver um tamponamento cardíaco comprovado ou altamente suspeito do ponto de vista clínico |
|
Hipoglicemia |
Insuficiência adrenal, abuso de álcool, superdosagem de aspirina, diabetes, fármacos, toxinas, hepatopatia, doença renal, sepse, alguns tumores |
Considerar o contexto clínico e obter medidas de glicose pelo teste da picada no dedo ou teste imediato de glicemia (pode ser determinada em amostras usadas para medição de GSA) Se a glicose < 60 mg/dL, tratar do seguinte modo: 50 mL = 25 g de D50W, IV. Acompanhar os níveis de glicose intensivamente no pós-tratamento* |
|
Hipomagnesemia |
Abuso de álcool, queimaduras, cetoacidose diabética, diarreia severa, diuréticos, fármacos (p. ex., cisplatina, ciclosporina, pentamidina), má absorção, ingesta precária, tireotoxicose |
Obter a medida imediata dos níveis séricos de magnésio Tratamento: 1 a 2 g de sulfato de magnésio IV, durante cerca de 5 min, para pacientes com FV ou TV sem pulso no contexto de suspeita de problemas de QT prolongado, torsade de pointes ou hipomagnesemia; acompanhar os níveis de magnésio com o passar do tempo, pois os níveis sanguíneos estão fracamente correlacionados com o déficit corporal total |
|
Hipotermia |
Abuso de álcool, queimaduras, doença do sistema nervoso central, pacientes debilitados e idosos, afogamento, fármacos, toxinas, endocrinopatia, história de exposição, sem teto, pobreza, doença extensa na pele, doença na medula espinal, traumatismo |
Obter a temperatura corporal central Se houver hipotermia severa (< 30°C), limitar a aplicação inicial dos choques em casos de TV sem pulsação/FV a uma só, iniciar o reaquecimento interno ativo e o suporte cardiopulmonar, e suspender as medicações ou choque adicionais de ressuscitação até a temperatura central se tornar > 30°C† Diante de uma hipotermia moderada (30 a 34°C), proceder à ressuscitação (espaçar as medicações a intervalos maiores do que o habitual), fornecer reaquecimento externo ativo (p. ex., ar forçado, infusões aquecidas) |
|
Hipovolemia, hemorragia, anemia |
Queimaduras significativas, diabetes, perdas gastrintestinais, hemorragia, diátese hemorrágica, malignidade, gestação, choque, traumatismo |
Iniciar a ressuscitação com grandes volumes de cristaloide IV Determinar os níveis de hemoglobina em amostra de gasometria arterial Em caráter emergencial, transfundir concentrado de hemácias (O negativo, se não houver sangue de tipo específico disponível) se uma hemorragia ou anemia profunda estiverem contribuindo para a parada Em caráter de emergência, consultar as especialidades necessárias para instituição de um tratamento definitivo A toracotomia emergencial com massagem cardíaca aberta pode ser considerada, desde que haja profissionais experientes disponíveis para atender um paciente com traumatismo de tronco com perfuração e parada cardíaca |
|
Hipóxia |
Todos os pacientes em parada cardíaca apresentam risco |
Reavaliar a qualidade técnica da RCP, oxigenação e ventilação Confirmar a correta colocação do tubo ET Obter a medida imediata de gasometria arterial para confirmar a adequação da oxigenação e da ventilação |
|
Infarto do miocárdio |
Considerar todos os pacientes em parada cardíaca, especialmente aqueles com fatores de risco para doença arterial coronariana, história de cardiopatia isquêmica ou quadro pré-parada consistente com síndrome coronariana aguda |
Rever a apresentação clínica e o ECG pré-parada Continuar o algoritmo de ressuscitação; prosseguir com o tratamento definitivo, conforme exigirem as circunstâncias imediatas (p. ex., terapia trombolítica, cateterismo cardíaco/reperfusão arterial coronariana, dispositivo auxiliar circulatório, desvio cardiopulmonar emergente) |
|
Envenenamento |
Abuso de álcool, manifestação metabólica ou comportamental bizarra ou embaraçosa, síndrome tóxica clássica, exposições ocupacionais ou industriais, história de ingesta, abuso de polifarmácia ou outras substâncias, doença psiquiátrica |
Considerar o contexto e a apresentação clínica; fornecer um tratamento de suporte meticuloso Consultar o toxicologista em caráter emergencial (via centro de envenenamentos regional) para obter conselhos sobre ressuscitação e tratamento definitivo, inclusive o uso apropriado de antídoto Os esforços de ressuscitação prolongados são apropriados; quando disponível, deve ser considerado o uso de circulação extra-corpórea. |
|
Hipercalemia |
Acidose metabólica, administração excessiva, fármacos e toxinas, exercício vigoroso, hemólise, doença renal, rabdomiólise, síndrome da lise tumoral, lesão tecidual significativa |
Obter a medida imediata dos níveis séricos de potássio em amostra de gasometria arterial. Tratamento: cloreto de cálcio a 10% (injeção IV lenta de 5 a 10 mL [não usar, se a hipercalemia for secundária ao envenenamento por digital]), seguido de glicose e insulina (50 mL de D50W e 10 U de insulina regular, IV); bicarbonato de sódio (50 mEq, IV); albuterol (nebulização de 15 a 20 mg ou infusão IV de 0,5 mg)‡ |
|
Hipocalemia |
Abuso de álcool, diabetes, uso de diurético, fármacos e toxinas, perdas gastrintestinais profundas, hipomagnesemia, condições de excesso de mineralocorticoide, alcalose metabólica |
Obter a medida imediata dos níveis séricos de potássio em amostra de gasometria arterial. Se houver uma hipocalemia profunda (IC+ < 2 a 2,5 mEq/L) que esteja contribuindo para a parada cardíaca, iniciar uma reposição IV urgente (2 mEq/min, IV, para alcançar 10 a 15 mEq); reavaliar em seguida§ |
|
Embolia pulmonar |
Pacientes internados, procedimento cirúrgico recente, periparto, fatores de risco comprovados para TEV, história de TEV, manifestação pré-parada consistente com embolia pulmonar aguda |
Rever o quadro clínico pré-parada; iniciar uma ressuscitação de volume apropriada, com cristaloide IV, e intensificar com vasopressores quando for necessário Tentar obter uma confirmação emergencial do diagnóstico, dependendo da disponibilidade e das circunstâncias clínicas; considerar uso de circulação extra-corpórea para manter a viabilidade do paciente. Continuar o algoritmo de ressuscitação; prosseguir com o tratamento definitivo (p. ex., terapia trombolítica, embolectomia por radiologia interventiva, ou trombectomia cirúrgica), conforme ditado pelas circunstâncias e disponibilidade imediata |
|
Pneumotórax por tensão |
Colocação de linha pós-central, ventilação mecânica, doença pulmonar (incluindo asma, DPOC, pneumonia necrotizante), pós-toracocentese, traumatismo |
Considerar os riscos e o quadro clínico (história pré-parada, sons respiratórios, veias cervicais, desvio traqueal) Proceder à descompressão emergencial com agulha, seguida da inserção de tubo no tórax |
*Uma hipoglicemia não identificada pode causar lesão neurológica significativa e também pode ser prejudicial à vida, porém a cautela com a administração IV de glicose é apropriada no contexto de parada cardíaca. As evidências disponíveis indicam que a hiperglicemia pode contribuir para a recuperação neurológica comprometida em sobreviventes de parada cardíaca.
†O reaquecimento ativo interno ou central inclui o fornecimento de oxigênio umidificado aquecido (42 a 46°C) através de um tubo ET; fornecimento de líquidos aquecidos por via IV; lavagem peritoneal; tubos de reaquecimento esofágico; lavagem da bexiga; e reaquecimento extracorporal, quando imediatamente disponível. O reaquecimento externo ativo inclui o uso de perolas de aquecimento, ar quente forçado, garrafas de água quente, coxins de aquecimento colocados sobre a virilha/pescoço/axila, e fontes irradiadoras de calor aplicadas externamente ao paciente.
‡A glicose inicialmente é desnecessária, se o paciente já estiver hiperglicêmico. Contudo, os níveis de glicose devem ser seguidos atentamente após a administração IV de insulina, devido ao risco de hipoglicemia (sobretudo e pacientes com insuficiência renal, devido à longa duração da ação da insulina IV nestes pacientes). O bicarbonato de sódio é mais útil para pacientes com acidose metabólica concomitante, e é menos efetivo para redução dos níveis séricos de potássio em pacientes com insuficiência renal dependentes de diálise. Altas doses de albuterol nebulizado devem diminuir os níveis séricos de potássio em 0,5 a 1,5 mEq/L dentro de 30 a 60 min, porém sua administração durante uma parada cardíaca pode ser difícil.
§Em uma situação de parada não cardíaca, as diretrizes usuais para reposição IV de potássio destinadas aos pacientes que necessitam de terapia parenteral em geral são de 10 a 20 mEq/h, com monitoramento ECG contínuo. Se houver uma hipocalemia grave contribuindo para a parada cardíaca, todavia, estas taxas de reposição usuais tornam-se impraticáveis, dada a natureza grave da situação. Nestas circunstâncias, a administração de cloreto de potássio (2 mEq/min, IV, para obter 10 a 15 mEq) é razoável, porém a reavaliação e atenção intensiva às mudanças de níveis, redistribuição e circunstâncias clínicas em curso são essenciais para prevenir o desenvolvimento de uma hipercalemia prejudicial à vida.
D50W = dextrose a 50% em água; DPOC = doença pulmonar obstrutiva crônica; ECG = eletrocardiograma; ET = endotraqueal; FV = fibrilação ventricular; GSA = gasometria arterial; IV = via endovenosa; RCP = ressuscitação cardiopulmonar; TEV = tromboembolia venosa; TV = taquicardia ventricular.
Ressuscitação cardíaca baseada nos achados de ritmo
Quando um monitor-desfibrilador chega à cena de uma parada cardíaca, o ritmo do paciente é imediatamente analisado. Esta etapa constitui a parte inicial do estágio de desfibrilação (ou etapa D) do levantamento primário da AHA. Existem 4 possibilidades de ritmo [Figura 1]: (1) TV sem pulso; (2) FV; (3) atividade elétrica organizada ou semi-organizada, mesmo na ausência de uma pulso carotídeo palpável, definindo uma AESP; e (4) assístolia. O manejo detalhado destes diferentes cenários de ressuscitação cardíaca baseia-se nas recomendações da AHA52 e do International Liaison Committee on Resuscitation.74 Estas recomendações foram revisadas nas diretrizes de 2005.75 Ao seguir estas diretrizes, o clínico deve lembrar que, com exceção da RCP inicial e da desfibrilação inicial para FV e TV sem pulsação, muitas destas recomendações que constituem a base da ressuscitação moderna são sustentadas por evidências ou baseadas em consenso (e não baseadas em evidências, como seria o ideal). Devido à natureza da parada cardíaca e às múltiplas variáveis envolvidas, é excepcionalmente difícil conduzir pesquisas de alta qualidade e prospectivamente delineadas sobre ressuscitação cardíaca.
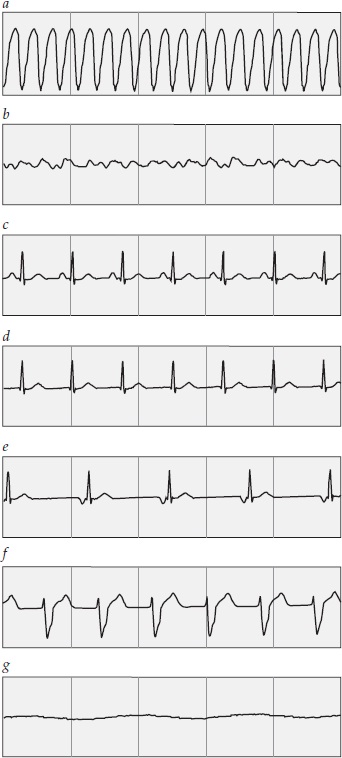
Figura 1. Arritmias da parada cardíaca súbita. (a) Taquicardia ventricular (TV). (b) Fibrilação ventricular (FV). A atividade elétrica sem pulsação (AESP) abrange qualquer uma dentre várias formas de atividade elétrica organizada em um paciente sem pulsação. Estas, por sua vez, incluem (c) o ritmo sinusal normal, (d) o ritmo juncional, (e) o ritmo juncional bradicárdico, e (f) o ritmo idioventricular. (g) Assístole.
Taquicardia ventricular (TV) sem pulsação ou fibrilação ventricular (FV)
O aspecto de uma FV ou de uma TV sem pulsação no monitor de ritmo, enquanto o paciente está recebendo uma RCP, é um achado relativamente favorável, pois há esperanças razoáveis de um resultado bem-sucedido associadas a estes ritmos. Além disso, as intervenções e medicações usadas em sequência na ressuscitação são claramente delineadas, com um curso de ação inicial nítido. A FV e a TV sem pulso são tratadas de modo idêntico.
Início da desfibrilação
A desfibrilação com 120 a 200 J (bifásica) ou 360 J (monofásica) deve ser tentada imediatamente. Entretanto, se a estimativa do intervalo de tempo entre o aparecimento da parada e a instituição da RCP até a disponibilização do desfibrilador for superior a 5 minutos, é razoável prosseguir com a RCP por mais 2 a 3 minutos antes de iniciar a desfibrilação [ver Desfibrilação, anteriormente]. Diferentemente das diretrizes antigas, todavia, as atuais diretrizes recomendam que após um tentativa de desfibrilação, a RCP deve ser reiniciada imediatamente. Não deve ser feita nenhuma tentativa de avaliar a resposta do ritmo à desfibrilação ou o retorno da circulação espontânea antes da conclusão de 5 ciclos de RCP (ou após cerca de 2 min de RCP em pacientes intubados). O objetivo desta recomendação é minimizar as pausas desnecessárias na compressão torácica, que caracterizaram as ressuscitações no passado. Se a FV ou a TV persistir após o choque inicial (seguido de 5 ciclos de RCP), então outra tentativa de desfibrilação deve ser realizada com 120 a 200 J (bifásica) ou 360 J (monofásica), também seguida imediatamente da realização de 5 ciclos de RCP e, então, da avaliação da resposta de ritmo ao choque [Figura 2].
Um nível de energia bifásico mais baixo, não escalado e equivalente é uma opção aceitável, desde que o desfibrilador ofereça esta alternativa. Após o choque seguido de 5 ciclos de RCP, o ritmo exibido no monitor deve ser cuidadosamente avaliado. Se o ritmo aparentemente for um ritmo de perfusão em potencial, a pulsação carotídea do paciente deve ser checada para confirmar o retorno da circulação espontânea. Se FV ou a TV sem pulso persistir, a RCP deve ser finalizada imediatamente, o paciente deve ser submetido á intubação ET, a correta colocação do tubo ET deve ser confirmada, e o tubo deve ser fixado. Ao mesmo tempo, o acesso IV deve ser estabelecido. Após a intubação, choques subsequentes para FV ou TV sem pulso devem ser aplicados grosso modo a cada 2 minutos. Mais uma vez, após a aplicação de cada choque, deve-se finalizar a RCP e não fazer avaliações de mudança de ritmo nem da presença de pulsação até que a RCP tenha sido fornecida por cerca de 2 minutos.
Início da terapia farmacológica
Em casos de pacientes com FV em curso, a terapia farmacológica é iniciada com um vasoconstritor (adrenalina ou vasopressina) [Tabela 4]. O fármaco é administrado tão logo o acesso IV seja estabelecido. Na ausência de um acesso IV, o fármaco pode ser administrado por via ET. Após a administração de cada dose IV de fármaco, administra-se um bolo de 20 mL de salina, e o membro que contém a linha IV é elevado. A administração de fármaco pode preceder ou seguir-se à aplicação do choque. Enquanto o paciente estiver sem pulsação, a adrenalina é administrada a cada 3 a 5 minutos. Quando a vasopressina é o fármaco de escolha inicial, somente uma única dose é administrada. Se a ressuscitação prosseguir por 10 minutos ou mais após a administração da vasopressina, então a adrenalina (1 mg, IV, a cada 3 a 5 min) deve ser substituída pela vasopressina para o restante do código. Caso a FV ou TV sem pulso persista mesmo após a administração inicial de um vasoconstritor e de tentativas repetidas de desfibrilação, então é adicionada uma terapia farmacológica antiarrítmica parenteral. A amiodarona ou a lidocaína são agentes apropriados [ver Escolha do fármaco antiarrítmico, adiante]. A administração do fármaco antiarrítmico pode preceder ou suceder uma tentativa de desfibrilação. No decorrer de todas estas etapas, o líder da equipe codificada também está ativamente procurando e corrigindo quaisquer problemas técnicos e fisiológicos ou anatômicos que possam estar impedindo o sucesso de uma ressuscitação [Tabelas 6 e 7].
Nota do editor: No caso se prefere amiodarona em relação a lidocaína.
Exames laboratoriais de emergência
Se a circulação espontânea não retornar após a 1ª ciclo de terapia farmacológica antiarrítmica, a equipe de ressuscitação deve esforçar-se para identificar e tratar condições clinicamente relevantes que estejam causando ou contribuindo para a parada cardíaca [Tabela 7]. Teoricamente, as intervenções conduzidas até este ponto já devem ter resultado em um ritmo de perfusão. A equipe de atendimento deve-se perguntar por que o retorno não aconteceu e, então, tentar responder esta pergunta enquanto a ressuscitação continua. Os exames laboratoriais de emergência que podem ser úteis incluem uma medida imediata de GSA e determinações dos níveis de hemoglobina, potássio, magnésio e glicemia (a maioria dos quais pode ser obtida a partir de uma amostra para GSA).
Escolha do fármaco antiarrítmico
Existem 3 fármacos que são usados na ressuscitação cardíaca no contexto de FV ou TV sem pulsação: amiodarona, lidocaína e magnésio (este último é usado se o paciente for considerado ou comprovadamente tiver hipomagnesemia, torsade de pointes ou um intervalo QT prolongado pré-parada).76 Não se sabe qual destes fármacos ou qual combinação destes fármacos otimizará as chances do paciente de sobreviver até a alta hospitalar. Embora a lidocaína seja usada há muitos anos, nenhum estudo controlado demonstrou os benefícios promovidos por este fármaco vs. um placebo no tratamento da FV ou da TV sem pulsação. Em 2 estudos envolvendo pacientes com FV pré-hospitalar refratária ao choque, demonstrou-se que a sobrevivência à admissão hospitalar foi melhor com o tratamento à base de amiodarona do que com placebo (44% vs. 34%; P = 0,03)77 ou lidocaína (22,8% vs. 12%; P = 0,009).78 Nenhum destes estudos demonstrou uma melhora da sobrevida até a alta hospitalar nos grupos de pacientes tratados com amiodarona, contudo nenhum estudo apresentou poder estatístico para demonstrar tal diferença. A amiodarona é consideravelmente mais cara do que a lidocaína.
O papel ideal e o benefício exato proporcionado pelas medicações antiarrítmicas na ressuscitação cardíaca ainda precisam ser totalmente elucidados. De acordo com as diretrizes da AHA, a amiodarona ou a lidocaína são ambas aceitáveis como fármacos antiarrítmicos iniciais para uso no tratamento de pacientes com FV ou TV sem pulsação irresponsiva ao choque inicial, RCP, manejo de vias aéreas e administração de adrenalina ou vasopressina + choques. Com base nas evidências disponíveis, todavia, a amiodarona pode ser o antiarrítmico de 1ª escolha no contexto de uma FV refratária pré-hospitalar, proporcionando ótima sobrevida até a chegada ao hospital.76-78
Atividade elétrica sem pulso (AESP)
Nos Estados Unidos, os prestadores de ACLS da comunidade estão se deparando com um número cada vez maior de casos de arritmia não ventricular (isto é, AESP e assístolia). Classicamente, o prognóstico da AESP é precário, com taxas de sobrevida ambulatorial em geral relatadas em 0 a 7%.79,80 No contexto hospitalar, apena 11% das vítimas adultas de parada com AESP sobrevivem até a alta hospitalar.11 A sequência de etapas da ressuscitação no manejo da AESP é a seguinte: ativação da emergência médica ou resposta de código; levantamento primário (RCP e avaliação do ritmo) e levantamento secundário (intubação e confirmação da correta colocação do tubo ET; oxigenação e ventilação ideais; estabelecimento de acesso IV; administração de adrenalina ou vasopressina; e, por fim, solução de problemas para dificuldades técnicas e estabelecimento da causa da parada cardíaca) [Figura 2]. Os fármacos centrais para tratamento da AESP são a adrenalina (repetida a cada 3 a 5 min, enquanto o paciente estiver sem pulsação) ou a vasopressina (40 UI, injeção IV, uma única dose) e atropina (até 3 mg com o passar do tempo, se o ritmo de AESP observado no monitor estiver inadequadamente lento). A melhor esperança de uma ressuscitação bem-sucedida consiste em encontrar e tratar a causa da AESP. É nisto que reside o aspecto excepcionalmente desafiador do manejo da ressuscitação da AESP [Tabelas 6 e 7]. Como a trombose arterial coronariana e a tromboembolia pulmonar são causas comuns de parada cardíaca, um estudo avaliou a eficácia do ativador de plasminogênio tecidual (t-PA) no contexto de AESP de causa cardiovascular desconhecida ou provável, em 233 pacientes em condição pré-hospitalar e atendidos no departamento de emergência.81 Neste estudo, a terapia trombolítica não promoveu nenhum benefício para os pacientes com AESP. A proporção de pacientes que apresentaram retorno da circulação espontânea foi de 21,4% no grupo tratado com t-PA e de 23,3% no grupo placebo.
Assístolia
O prognóstico para a assístolia em geral é considerado ruim, exceto nos casos de pacientes hipotérmicos ou diante de outras circunstâncias extenuantes, porém tratáveis. Entre as vítimas de assístole que sofrem parada cardíaca internadas no hospital, a taxa de sobrevida à alta hospitalar é de cerca de 10%.11 A sequência de etapas de ressuscitação do manejo da assístolia é a seguinte: ativação da equipe de emergência médica ou de código azul, em hospitais com esta equipe (um socorrista solitário que se depara com provável caso de parada por asfixia deve realizar 5 ciclos de RCP antes de ativar o serviço de atendimento de emergência); atendimento primário (RCP, avaliação do ritmo e confirmação da assístole) e atendimento secundário (intubação e confirmação da correta colocação do tubo ET; oxigenação e ventilação ideais; estabelecimento de acesso IV; administração de adrenalina ou vasopressina e atropina; uso imediato de marca-passo transcutâneo (quando disponível); e solução de problemas para dificuldades técnicas e estabelecimento da causa da parada cardíaca) [Figura 2]. Os fármacos centrais para tratamento da assístolia são a adrenalina (repetida a cada 3 a 5 min, enquanto o paciente estiver sem pulsação) ou a vasopressina (40 UI, injeção IV) aliada à atropina (até 3 mg com o passar do tempo). Assim como para os pacientes com AESP, a vasopressina parece ser razoável e possivelmente benéfica como substituto da adrenalina na assístole. Uma única dose de aminofilina (250 mg, IV) também pode ser benéfica em casos de assístolia atropina-resistente.82 As causas potencialmente tratáveis da assístolia incluem hipóxia, acidose, hipotermia, hipocalemia, hipercalemia e superdosagem de fármaco. Os esforços de ressuscitação devem ser interrompidos quando a assístolia persistir por mais de 10 minutos, mesmo após o estabelecimento de condições ideais de RCP, oxigenação e ventilação, e administração de adrenalina ou vasopressina e atropina; na ausência de circunstâncias extenuantes (p. ex., hipotermia, submersão em água fria ou superdosagem de fármaco); e se nenhuma outra condição prontamente tratável for identificada.
Tratamento pós-ressuscitação imediato
Até mesmo quando a ressuscitação é bem-sucedida, a situação do paciente permanece tênue e é essencial que ele(a) continue recebendo um tratamento meticuloso. Quando o monitor cardíaco indica aquilo que deveria ser um ritmo de perfusão, o resgatador deve confirmar imediatamente se o paciente apresenta pulso palpável. Se o pulso estiver presente, então a pressão arterial do paciente deve ser medida. Ao mesmo tempo, os membros da equipe de ressuscitação precisam reavaliar rapidamente a adequação das vias aéreas do paciente, a posição do tubo ET, a oxigenação e ventilação, e o nível de consciência e conforto do paciente.
Se o paciente estiver hipotensivo, o manejo adequado da pressão arterial dependerá da presença ou ausência de sobrecarga líquida, conforme o julgamento à beira do leito. Se, clinicamente, o paciente apresentar sobrecarga de líquido ou um edema pulmonar franco e estiver hipotenso, um curso de dopamina deve ser iniciado com doses inotrópicas (5 mcg/kg/min, IV) e titulado para uma pressão arterial sistólica-alvo de 90 a 100 mmHg. Se a condição clínica do paciente sugerir normovolemia ou hipovolemia, é possível administrar bolos de cristaloide IV (com incrementos de 250 a 500 mL), em vez da dopamina, para otimizar o volume intravascular e sustentar uma perfusão tecidual adequada. No caso dos pacientes que estão voltando à consciência, o nível de conforto deles exige a realização de uma avaliação detalhada e da administração de analgesia e sedação, de acordo com a necessidade.
Nota do editor: Estudos recentes tornam a norepinefrina a droga vasopressora de escolha na maioria das situações e nao mais a dopamina.
Se o ritmo de parada for TV ou FV, o fármaco antiarrítmico parenteral administrado imediatamente antes do retorno da circulação espontânea é continuado como infusão de manutenção (1 mg de amiodarona/min, durante 6 horas, seguida de 0,5 mg de amiodarona/min, por mais 18 horas, conforme a pressão arterial permitir; ou, ainda, 2 a 4 mg de lidocaína/min). Caso um fármaco antiarrítmico ainda não tenha sido administrado, um curso em geral é iniciado neste momento, com o intuito de prevenir a recorrência da FV ou da TV sem pulso. Contudo, existem exceções importantes a esta diretriz. Se a arritmia pós-parada perfusiva for um ritmo idioventricular ou um bloqueio cardíaco de 3º grau acompanhado de ritmo de escape idioventricular, uma medicação antiarrítmica não deve ser iniciada neste momento, porque o agente antiarrítmico poderia eliminar o foco de perfusão ventricular e fazer o paciente voltar à condição de ausência de pulsação.
Os exames pós-ressuscitação iniciais incluem um ECG; radiografia torácica portátil; e medida de GSA, painel de eletrólitos séricos, teste de glicose no sangue ou teste da picada do dedo, níveis séricos de magnésio e níveis de enzimas cardíacas, além de concentração de hemoglobina e hematócrito. O paciente ressuscitado necessita de transferência urgente para um estabelecimento ideal, para que possa receber um tratamento definitivo e contínuo. Dependendo das circunstâncias, este local pode ser um laboratório de cateterismo cardíaco ou a unidade de terapia intensiva (UTI).
As pesquisas atualmente conduzidas continuam buscando estratégias de manejo pós-ressuscitação ideais que melhorem o resultado neurológico e a sobrevida dos pacientes à alta hospitalar.83 A hipertermia e a hiperglicemia comprometem o resultado neurológico pós-ressuscitação, enquanto a hipotermia induzida leve a moderada parece melhorar o resultado neurológico e diminuir a mortalidade.84-87
Finalizando uma tentativa de ressuscitação
Ao longo de toda a ressuscitação, o líder da equipe deve falar com calma e autoridade, e todas as ressuscitações devem ser orquestradas com clareza e destreza. Quando possível, o líder da equipe deve tomar as decisões clínicas sem realizar diretamente os procedimentos específicos. Quando um procedimento é executado ou um fármaco é administrado, o membro da equipe deve comunicar imediatamente ao líder da equipe a conclusão da ordem (p. ex., “1 mg de adrenalina acabou de ser administrado como injeção IV”). As paradas cardíacas são carregadas de emoção, contudo o líder deve insistir para que a ressuscitação seja conduzida de modo composto, ordenado e tecnicamente sólido. Convém aceitar sugestões dos membros da equipe e garantir que todos se sintam confortáveis com a decisão de parar a ressuscitação, quando chegar a hora de fazer isto.
A decisão de finalizar a ressuscitação cardíaca é onerosa. Nitidamente, as circunstâncias do evento, comorbidades do paciente, natureza da arritmia letal e habilidade da equipe de ressuscitação de identificar e tratar corretamente as potenciais causas que contribuem para a circunstância da parada são todas considerações importantes. As tentativas de ressuscitação que duram mais de 30 minutos e não obtêm o retorno da circulação espontânea geralmente são inúteis, a menos que a parada cardíaca seja confundida por FV recorrente ou TV sem pulso, hipotermia, submersão em água fria, superdosagem de fármaco ou outras condições contribuintes identificadas e prontamente tratáveis.88,89
No caso da parada cardíaca não traumática no contexto pré-hospitalar (considerando que há disponibilidade de equipamento adequado e medicações, sem nenhuma circunstância extenuante sugestiva do contrário), os esforços de ressuscitação integrais são iniciados na cena da parada, de preferência para que o paciente seja rapidamente transportado até um departamento de emergência. Uma ressuscitação pré-hospitalar que tenha sido corretamente conduzida sem, contudo, resultar nem mesmo no retorno temporário da circulação espontânea do paciente pode ser finalizada ainda em campo. Entretanto, é importante a adesão a certos critérios, os quais incluem: realizar uma RCP de alta qualidade e com o mínimo possível de interrupções; colocar uma via respiratória adequada e de maneira bem-sucedida; fornecer oxigenação e ventilação adequadas; estabelecer o acesso IV; administrar medicações apropriadas específicas para o cenário da parada; e tentar a ressuscitação durante pelo menos 10 minutos. Além disso, o paciente não pode permanecer em FV persistente e não deve haver circunstâncias extenuantes que obriguem a continuação da ressuscitação no hospital (p. ex., hipotermia, superdosagem de fármacos). A decisão de cessar as tentativas de ressuscitação em campo ganha sustentação com uma discussão direta com os médicos do atendimento de emergência. Também é essencial contar com serviços sociais disponíveis que forneçam assistência e suporte imediato à família e aos entes queridos do paciente que acabou de morrer.
A descontinuação das ressuscitações no hospital é recomendável para os casos que atendem a 3 critérios: (1) a parada não foi testemunhada; (2) o ritmo inicial não era FV nem TV; e (3) a circulação espontânea não retornou após 10 minutos de tentativas de ressuscitação.36 Em um estudo sobre esta regra de 3 componentes, apenas 1,1% dos pacientes (3 em 269) que atenderam a estes critérios sobreviveram à alta hospitalar, sendo que nenhum destes 3 sobreviventes conseguiu viver de maneira independente.90 Em um estudo sobre 445 tentativas de ressuscitação de pacientes internados prospectivamente registradas, não houve sobreviventes entre os pacientes que haviam sofrido parada cardíaca entre meia-noite e 6 horas da manhã, quando a parada não foi testemunhada e quando ocorreu em leito não monitorado.40
Uma tentativa de ressuscitação em um paciente persistentemente em assistolia não deve durar mais que 10 minutos, considerando-se aplicáveis todas as seguintes condições: a assístole está confirmada via monitoramento e avaliação apropriada do ritmo; uma RCP de alta qualidade está sendo fornecida, com o mínimo possível de interrupções; uma intubação ET está sendo realizada e confirmada; uma oxigenação e ventilação adequada estão sendo fornecidas; o acesso IV está fixo; as medicações apropriadas (atropina e adrenalina ou vasopressina) foram administradas; e o paciente não é vítima de hipotermia, submersão em água fria, superdosagem de fármaco ou outra causa prontamente identificada e reversível.
Após todas as tentativas de ressuscitação, o líder da equipe deve fazer o relatório da equipe, de modo que todos possam aprender com a experiência. Por fim, é preciso usar de acentuada empatia e habilidade para comunicar com cuidado e compaixão aos familiares do paciente o resultado da tentativa de ressuscitação.91
Nota do editor: Este capítulo do ACP Medicine foi baseado nas recomendações do ACLS ainda de 2005, assim algumas mudanças na sistematização do atendimento, muitas delas pontuadas pelo editor brasileiro, ainda assim por ser um texto muito rico, foi disponibilizado para os assinates do site.
O autor não possui relações comerciais com os fabricantes de produtos e prestadores de serviço mencionados neste capítulo.
Referências
1. Callans DJ: Management of the patient who has been resuscitated from sudden cardiac death. Circulation 105:2704, 2002
2. Zipes DP, Wellens HJ: Sudden cardiac death. Circulation 98:2334, 1998
3. Eisenberg MS, Mengert TJ: Cardiac resuscitation. N Engl J Med 344:1304, 2001
4. 1999 Heart and Stroke Statistical Update. American Heart Association, Dallas, 1998
5. Huikuri HV, Castellanos A, Myerburg R: Sudden death due to cardiac arrhythmias. N Engl J Med 345:1473, 2001
6. Ballew KA, Philbrick JT: Causes of variation in reported in-hospital CPR survival: a critical review. Resuscitation 30:203, 1995
7. Myerburg RJ, Castellanos A: Cardiac arrest and sudden cardiac death. Heart Disease: A Textbook of Cardiovascular Medicine. Braunwald E, Ed. WB Saunders Co, Philadelphia, 1997, p 742
8. Osborn LA: Etiology of sudden death. Cardiac Arrest: The Science and Practice of Resuscitation Medicine. Paradis NA, Halperin HR, Nowak RM, Eds. Williams & Wilkins, Philadelphia, 1996, p 243
9. Maron BJ: Sudden death in young athletes. N Engl J Med 349:1064, 2003
10. Cobb LA, Fahrenruch CD, Olsufka M, et al: Changing incidence of out-of-hospital ventricular fibrillation, 1980–2000. JAMA 288:3008, 2002
11. Nadkarni VM, Larkin GL, Peberdy MA, et al: First documented rhythm and clinical outcome from in-hospital cardiac arrest among children and adults. JAMA 295:50, 2006
12. Cummins RO, Ornato JP, Thies W, et al: Improving survival from cardiac arrest: the chain of survival concept: a statement for health professionals from the Advanced Cardiac Life Support Subcommittee and the Emergency Cardiac Care Committee, American Heart Association. Circulation 83:1832, 1991
13. 2005 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Part 4: adult basic life support. ECC Committee, Subcommittees and Task Forces of the American Heart Association. Circulation 112(24 suppl):IV19, 2005
14. Capussi A, Aschieri D, Piepoli MF, et al: Tripling survival from sudden cardiac arrest via early defibrillation without traditional education in cardiopulmonary resuscitation. Circulation 106:1065, 2002
15. Callaham M, Madsen CD: Relationship of timeliness of paramedic advanced life support interventions to outcome in out-of-hospital cardiac arrest treated by first responders with defibrillators. Ann Emerg Med 27:638, 1996
16. Marenco JP, Wang PJ, Link MS, et al: Improving survival from sudden cardiac arrest: the role of the automated external defibrillator. JAMA 285:1193, 2001
17. Peberdy MA: Defibrillation. Cardiol Clin 20:13, 2002
18. Public-access defibrillation and survival after out-of-hospital cardiac arrest. The Public Access Defibrillation Trial Investigators. N Engl J Med 351:637, 2004
19. Cummins RO, Eisenberg MS: Prehospital cardiopulmonary resuscitation: is it effective? JAMA 253:2408, 1985.
20. Stapleton ER: Basic life support cardiopulmonary resuscitation. Cardiol Clin 20:12, 2002
21. Valenzuela TD, Roe DJ, Cretin S, et al: Estimating effectiveness of cardiac arrest interventions: a logistic regression survival model. Circulation 96:3308, 1997
22. Eisenberg MS, Bergner L, Hallstrom A: Cardiac resuscitation in the community: the importance of rapid delivery of care and implications for program planning. JAMA 241:1905, 1979
23. Weaver WD, Cobb LA, Hallstrom AP, et al: Considerations for improving survival from out-of-hospital cardiac arrest. Ann Emerg Med 15:1181, 1986
24. Larsen MP, Eisenberg MS, Cummins RO, et al: Predicting survival from out-of-hospital cardiac arrest: a graphic model. Ann Emerg Med 270:1211, 1993
25. Eisenberg MS, Horwood BT, Cummins RO, et al: Cardiac arrest and resuscitation: a tale of 29 cities. Ann Emerg Med 19:179, 1990
26. Lombardi G, Gallagher J, Gennis P: Outcome of out-of-hospital cardiac arrest in New York City: the Pre-Hospital Arrest Survival Evaluation (PHASE) study. JAMA 271:678, 1994
27. Becker LB, Ostrander MP, Barrett J, et al: Outcome of CPR in a large metropolitan area: where are the survivors? Ann Emerg Med 20:355, 1991
28. Killien SY, Geyman JP, Gossom JB, et al: Out-of-hospital cardiac arrest in a rural area: a 16-year experience with lessons learned and national comparisons. Ann Emerg Med 28:294, 1996
29. Bunch TJ, White RD, Gersh BJ, et al: Long-term outcomes of out-of-hospital cardiac arrest after successful early defibrillation. N Engl J Med 348:2626, 2003
30. Valenzuela TD, Roe DJ, Nichol G, et al: Outcomes of rapid defibrillation by security officers after cardiac arrest in casinos. N Engl J Med 343:1206, 2000
31. Eisenberg M, Bergner L, Hallstrom A: Sudden Cardiac Death in the Community. Praeger, Philadelphia, 1984
32. Becker L: The epidemiology of sudden death. Cardiac Arrest: The Science and Practice of Resuscitation Medicine. Paradis NA, Halperin HR, Nowak RM, Eds. Williams & Wilkins, Philadelphia, 1996, p 28
33. Jastremski MS: In-hospital cardiac arrest. Ann Emerg Med 22:113, 1993
34. Rosenberg M, Wang C, Hoffman-Wilde S, et al: Results of cardiopulmonary resuscitation: failure to predict survival in two community hospitals. Arch Intern Med 153:1370, 1993
35. Ballew KA, Philbrick JT, Caven DE, et al: Predictors of survival following in-hospital cardiopulmonary resuscitation: a moving target. Arch Intern Med 154:2426, 1994
36. de Vos R, Koster RW, de Haan RJ, et al: In-hospital cardiopulmonary resuscitation: prearrest morbidity and outcome. Arch Intern Med 159:845, 1999
37. Goodlin SJ, Zhong Z, Lynn J, et al: Factors associated with use of cardiopulmonary resuscitation in seriously ill hospitalized adults. JAMA 282:2333, 1999
38. van Walraven C, Forster AJ, Stiell IG: Derivation of a clinical decision rule for the discontinuation of in-hospital cardiac arrest resuscitations. Arch Intern Med 159:129, 1999
39. Zoch TW, Desbiens NA, DeStefano F, et al: Short- and long-term survival after cardiopulmonary resuscitation. Arch Intern Med 160:1969, 2000
40. Dumot JA, Burval DJ, Sprung J, et al: Outcome of adult cardiopulmonary resuscitations at a tertiary referral center, including results of “limited” resuscitations. Arch Intern Med 161:1751, 2001
41. Meade M: Men and the Water of Life. Harper, San Francisco, 1993, p 442
42. Burkle FM Jr, Rice MM: Code organization. Am J Emerg Med 5:235, 1987
43. ACLS Provider Manual. American Heart Association, Dallas, 2001
44. Safar P: On the history of modern resuscitation. Anesthesiol Clin North Am 13:751, 1995
45. Kouwenhoven WB, Jude JR, Knickerbocker GG: Closed-chest cardiac massage. JAMA 173:1064, 1960
46. Jude JR, Kouwenhoven WB, Knickerbocker GG: Cardiac arrest: report of application of external cardiac massage on 118 patients. JAMA 178:1063, 1961
47. Halperin HR: Mechanisms of forward flow during external chest compression. Cardiac Arrest: The Science and Practice of Resuscitation Medicine. Paradis NA, Halperin HR, Nowak RM, Eds. Williams & Wilkins, Philadelphia, 1996, p 252
48. Ornato JP, Peberdy MA: Cardiopulmonary resuscitation. Textbook of Cardiovascular Medicine. Topol EJ, Ed. Lippincott-Raven, Philadelphia, 1998, p 1779
49. Paradis NA, Martin GB, Goetting MG, et al: Simultaneous aortic, jugular bulb, and right atrial pressures during cardiopulmonary resuscitation in humans: insights into mechanisms. Circulation 80:361, 1989
50. Daya MR, Mariani RJ: Out-of-hospital splinting. Clinical Procedures in Emergency Medicine, 3rd ed. Roberts JR, Hedges JR, Eds. WB Saunders Co, Philadelphia, 1998, p 1297
51. Guidelines 2000 for cardiopulmonary resuscitation and emergency cardiovascular care: international consensus on science. Circulation 102(suppl I):1, 2000
52. 2005 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Part 3: overview of CPR. ECC Committee, Subcommittees and Task Forces of the American Heart Association. Circulation 112(24 suppl):IV12, 2005
53. Sanders AB, Kern KB, Berg RA, et al: Survival and neurologic outcome after cardiopulmonary resuscitation with four different chest compression–ventilation ratios. Ann Emerg Med 40:553, 2002
54. Hallstrom A, Cobb L, Johnson E, et al: Cardiopulmonary resuscitation by chest compression alone or with mouth-to-mouth ventilation. N Engl J Med 342:1546, 2000
55. Levine RL, Wayne MA, Miller CC: End-tidal carbon dioxide and outcome of out-ofhospital cardiac arrest. N Engl J Med 337:301, 1997
56. Hedges JR, Greenberg MI: Defibrillation. Clinical Procedures in Emergency Medicine, 3rd ed. Roberts JR, Hedges JR, Eds. WB Saunders Co, Philadelphia, 1998, p 1297
57. Hossack KF, Hartwig R: Cardiac arrest associated with supervised cardiac rehabilitation. J Cardiac Rehab 2:402, 1982
58. Bardy GH, Marchlinski FE, Sharma AD, et al: Multicenter comparison of truncated biphasic shocks and standard damped sine wave monophasic shocks for transthoracic ventricular defibrillation. Circulation 94:2507, 1996.
59. Gliner BE, White RD: Electrocardiographic evaluation of defibrillation shocks delivered to out-of-hospital sudden cardiac arrest patients. Resuscitation 41:129, 1999
60. Gliner BE, Jorgenson DB, Poole JE, et al: Treatment of out-of-hospital cardiac arrest with a low-energy impedance-compensating biphasic waveform automatic external defibrillator. Biomed Instrum Technol 32:631, 1998
61. Poole JE, White RD, Kanz KG, et al: Low-energy impedance-compensating biphasic waveforms terminate ventricular fibrillation at high rates in victims of out-of-hospital cardiac arrest. J Cardiovasc Electrophysiol 8:1373, 1997
62. Schneider T, Martens PR, Paschen H, et al: Multicenter, randomized, controlled trial of 150-J biphasic shocks compared with 200- to 360-J monophasic shocks in the resuscitation of out-of-hospital cardiac arrest victims. Circulation 102:1780, 2000
63. Berg RA, Hilwig RW, Kern KB, et al: Precountershock cardiopulmonary resuscitation improves ventricular fibrillation median frequency and myocardial readiness for successful defibrillation from prolonged ventricular fibrillation: a randomized, controlled swine study. Ann Emerg Med 40:563, 2002
64. Wik L, Hansen TB, Fylling F, et al: Delaying defibrillation to give basic cardiopulmonary resuscitation to patients with out-of-hospital ventricular fibrillation. JAMA 289:1389, 2003
65. Weisfeldt ML, Becker LB: Resuscitation after cardiac arrest: a 3-phase time sensitive model. JAMA 288:3035, 2002
66. Aehlert B: ACLS: Quick Review Study Guide, 2nd ed. CV Mosby, St Louis, 2001
67. Rumball CJ, MacDonald D: The PTL, Combitube, laryngeal mask, and oral airway: a randomized prehospital comparative study of ventilatory device effectiveness and cost-effectiveness in 470 cases of cardiorespiratory arrest. Prehosp Emerg Care 1:1, 1997
68. Garnett AR, Ornato JP, Gonzales ER, et al: End-tidal carbon dioxide monitoring during cardiopulmonary resuscitation. JAMA 257:512, 1987
69. Paradis NA, Wenzel V, Southall J: Pressor drugs in the treatment of cardiac arrest. Cardiol Clin 20:61, 2002
70. Stiell IG, Hebert PC, Wells GA, et al: Vasopressin versus epinephrine for inhospital cardiac arrest: a randomized controlled trial. Lancet 358:105, 2001
71. Wenzel V, Krismer AC, Arntz HR, et al: A comparison of vasopressin and epinephrine for out-of-hospital cardiopulmonary resuscitation. N Engl J Med 350:105, 2004
72. McIntryre KM: Vasopressin in asystolic cardiac arrest. N Engl J Med 350:179, 2004
73. Tiffany PA, Schultz M, Stueven H: Bolus thrombolytic infusions during CPR for patients with refractory arrest rhythms: outcome of a case series. Ann Emerg Med 31:124, 1998
74. Cummins RO, Chamberlain DA: Advisory statements of the International Liaison Committee on Resuscitation. Circulation 95:2172, 1997
75. 2005 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care, part 7: advanced cardiovascular life support. ECC Committee, Subcommittees and Task Forces of the American Heart Association. Circulation 112(24 suppl):IV51, 2005
76. Kudenchuk PJ: Advanced cardiac life support antiarrhythmic drugs. Cardiol Clin 20:79, 2002
77. Kudenchuk PJ, Cobb LA, Copass MK, et al: Amiodarone for resuscitation after outof-hospital cardiac arrest due to ventricular fibrillation. N Engl J Med 341:871, 1999
78. Dorian P, Cass D, Schwartz B, et al: Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med 346:884, 2002
79. Myerburg RJ, Conde CA, Sung RJ, et al: Clinical, electrophysiologic, and hemodynamic profile of patients resuscitated from prehospital cardiac arrest. Am J Med 68:568, 1980
80. Stratton SJ, Niemann JT: Outcome from out-of-hospital cardiac arrest caused by nonventricular arrhythmias: contribution of successful resuscitation to overall survivorship supports the current practice of initiating out-of-hospital ACLS. Ann Emerg Med 32:448, 1998
81. Abu-Laban RB, Christenson JM, Innes GD, et al: Tissue plasminogen activator in cardiac arrest with pulseless electrical activity. N Engl J Med 346:1522, 2002
82. Mader TJ, Smithline HA, Durkin L, et al: A randomized controlled trial of intravenous aminophylline for atropine-resistant out-of-hospital asystolic cardiac arrest. Acad Emerg Med 10:192, 2003
83. Angelos MG, Menegazzi JJ, Callaway CW: Bench to bedside: resuscitation from prolonged ventricular fibrillation. Acad Emerg Med 8:909, 2001
84. Zeiner A, Holzer M, Sterz F, et al: Hyperthermia after cardiac arrest is associated with an unfavorable neurological outcome. Arch Intern Med 161:2007, 2001
85. Moghissi E: Hospital management of diabetes: beyond the sliding scale. Cleve Clin J Med 71:801, 2004
86. Bernard SA, Gray TW, Buist MD, et al: Treatment of comatose survivors of out-ofhospital cardiac arrest with induced hypothermia. N Engl J Med 346:557, 2002
87. Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. The Hypothermia after Cardiac Arrest Study Group. N Engl J Med 346:549, 2002
88. Bonnin MJ, Pepe PE, Kimball KT, et al: Distinct criteria for termination of resuscitation in the out-of-hospital setting. JAMA 270:1457, 1993
89. Kellermann AL, Hackman BB, Somes G: Predicting the outcome of unsuccessful prehospital advanced cardiac life support. JAMA 270:1433, 1993
90. van Walraven C, Forster AJ, Parish DC, et al: Validation of a clinical decision aid to discontinue in-hospital cardiac arrest resuscitations. JAMA 285:1602, 2001
91. Iserson K: Grave Words: Notifying Survivors about Sudden, Unexpected Deaths. Galen Press, Tucson, Arizona, 1999
92. Cummins RO, Field JM, Hazinski MF, et al: ACLS Provider Manual. American Heart Association, Dallas, 2001, p 36
93. Part 1: introduction to the International Guidelines 2000 for CPR and ECC: a consensus on science. Circulation 102(8 suppl):I1, 2000