Arsenal Terapêutico no Suporte Hemoterápico
Reproduzido de:
Guia para o Uso de Hemocomponentes
Série A. Normas e Manuais Técnicos [Link Livre para o Documento Original]
MINISTÉRIO DA SAÚDE
Secretaria de Atenção à Saúde
Departamento de Atenção Especializada
Brasília / DF – 2008
2 Arsenal Terapêutico no Suporte Hemoterápico
Os hemocomponentes e hemoderivados se originam da doação de sangue por um doador. No Brasil, este processo está regulamentado pela Lei nº 10.205, de 21/3/2001, e por regulamentos técnicos editados pelo Ministério da Saúde. Toda doação de sangue deve ser altruísta, voluntária e não-gratificada direta ou indiretamente, assim como o anonimato do doador deve ser garantido.
Para a obtenção destes produtos, os serviços de hemoterapia são estruturados em rede, com níveis de complexidade diferentes, a depender das atividades que executam. Serviços mais completos executam todas as etapas do ciclo do sangue, que correspondem à captação de doadores, à triagem clínica, à coleta de sangue, ao processamento de sangue em hemocomponentes, às análises sorológicas e imuno-hematológicas no sangue do doador, ao armazenamento e à distribuição destes produtos e à transfusão.
As técnicas de processamento atuais permitem o armazenamento de diferentes hemocomponentes em condições adequadas para preservação de suas características terapêuticas, possibilitando que o receptor receba, em menor volume, somente hemocomponentes dos quais necessita, o que minimiza os riscos inerentes à terapêutica transfusional. Deste modo, a partir de uma única doação, vários pacientes poderão ser beneficiados de forma mais segura.
2.1 A PRODUÇÃO DOS HEMOCOMPONENTES
Hemocomponentes e hemoderivados são produtos distintos. Os produtos gerados um a um nos serviços de hemoterapia, a partir do sangue total, por meio de processos físicos (centrifugação, congelamento) são denominados hemocomponentes. Já os produtos obtidos em escala industrial, a partir do fracionamento do plasma por processos físico-químicos são denominados hemoderivados. A Figura 1 apresenta os produtos originados a partir do sangue total.
Existem duas formas para obtenção dos hemocomponentes. A mais comum é a coleta do sangue total. A outra forma, mais específica e de maior complexidade, é a coleta por meio de aférese[1].
No Brasil, as bolsas de sangue total coletadas devem ser 100% processadas de acordo com a Resolução da Diretoria Colegiada da Agência Nacional de Vigilância Sanitária RDC n° 24, de 24/1/2002. O processamento é feito por meio de centrifugação refrigerada, por processos que minimizam a contaminação e proliferação microbiana, nos quais se separa o sangue total em hemocomponentes eritrocitários, plasmáticos e plaquetários.
Figura 1: Produtos originados a partir do sangue total.
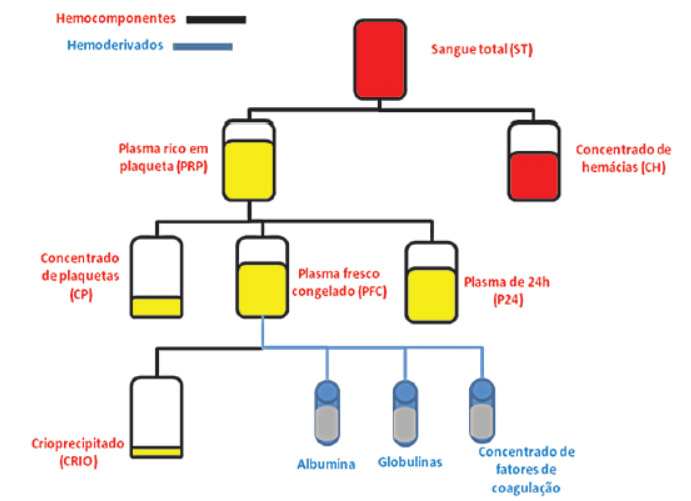
Fonte: adaptado de Brasil (1998).
Em função das diferentes densidades e tamanhos das células sanguíneas, o processo de centrifugação possibilita a separação do sangue total em camadas (Figura 2), sendo que as hemácias ficam depositadas no fundo da bolsa. Acima delas forma-se o buffy-coat (camada leucoplaquetária), ou seja, uma camada de leucócitos e plaquetas. Acima do buffy-coat fica a camada de plasma que contém plaquetas dispersas.
Figura 2: Separação do sangue total em camadas após a centrifugação.
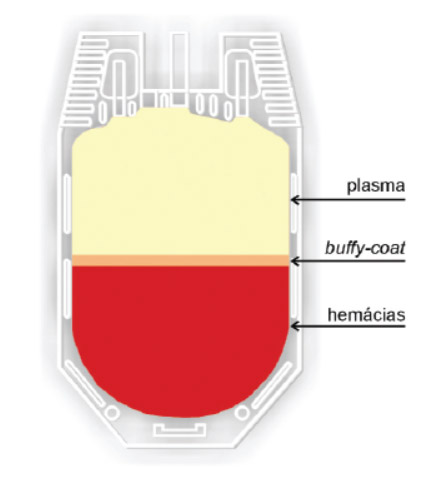
Fonte: Brasil (1998).
Soluções anticoagulantes-preservadoras e soluções aditivas são utilizadas para a conservação dos produtos sanguíneos, pois impedem a coagulação e mantêm a viabilidade das células do sangue durante o armazenamento. A depender da composição das soluções anticoagulantes-preservadoras, a data de validade para a preservação do sangue total e concentrados de hemácias pode variar. O sangue total coletado em solução CPDA-1 (ácido cítrico, citrato de sódio, fosfato de sódio, dextrose e adenina) tem validade de 35 dias a partir da coleta e de 21 dias quando coletado em ACD (ácido cítrico, citrato de sódio, dextrose), CPD (ácido cítrico, citrato de sódio, fosfato de sódio, dextrose) e CP2D (citrato, fosfato e dextrose-dextrose).
As soluções aditivas são utilizadas para aumentar a sobrevida e a possibilidade de armazenamento das hemácias por até 42 dias em 4 ± 2°C. Um exemplo de solução aditiva é o SAG-M composto por soro fisiológico, adenina, glicose e manitol.
2.1.1 Concentrado de Hemácias
O concentrado de hemácias (CH) é obtido por meio da centrifugação de uma bolsa de sangue total (ST) e da remoção da maior parte do plasma. Seu volume varia entre 220 ml e 280 ml.
Assim como o ST, o concentrado de hemácias deve ser mantido entre 2°C e 6°C e sua validade varia entre 35 e 42 dias, dependendo da solução conservadora. Os concentrados de hemácias sem solução aditiva devem ter hematócrito entre 65% e 80%. No caso de bolsas com solução aditiva, o hematócrito pode variar de 50% a 70%.
Os CH podem ser desleucocitados com a utilização de filtros para leucócitos ou desplamatizados pela técnica de lavagem com solução salina fisiológica preferencialmente em sistema fechado.
2.1.2 Concentrado de Plaqueta
O concentrado de plaquetas (CP) pode ser obtido a partir de unidade individual de sangue total ou por aférese, coletadas de doador único. Cada unidade de CP unitários contém aproximadamente 5,5 x 1010 plaquetas em 50-60 ml de plasma, já as unidades por aférese contém pelo menos 3,0 x 1011 plaquetas em 200-300 ml de plasma (correspondente de 6 a 8 unidades de CP unitários).
Dois métodos diferentes são utilizados para a obtenção de plaquetas pela centrifugação de sangue total. O primeiro consiste na centrifugação do sangue em duas etapas. Na primeira etapa, é feita uma centrifugação leve, em que se obtém o plasma rico em plaquetas (PRP); este plasma é novamente centrifugado, desta vez em alta rotação, para a obtenção do concentrado de plaquetas (CP).
O segundo método baseia-se na extração do buffy coat, ou camada leucoplaquetária, geralmente com a utilização de extratores automatizados de plasma e com o uso de bolsas top and bottom. O sangue total é submetido à centrifugação, visando à separação da camada leucoplaquetária. O plasma sobrenadante é transferido para uma bolsa-satélite, pela saída superior (top) da bolsa e o concentrado de hemácias é extraído pela saída inferior (bottom) da bolsa. A camada leucoplaquetária permanece na bolsa original.
O buffy coat de cada bolsa pode ser agrupado com outros por meio de metodologia estéril, seguido de sedimentação ou centrifugação para a separação e transferência das plaquetas para uma bolsa-satélite, onde ficam armazenadas em pool. Este método possibilita a redução no teor de leucócitos de aproximadamente 90% (1 log).
2.1.3 Plasma
O plasma fresco congelado (PFC) consiste na porção acelular do sangue obtida por centrifugação a partir de uma unidade de sangue total e transferência em circuito fechado para uma bolsa satélite. Pode ser obtido também a partir do processamento em equipamentos automáticos de aférese. É constituído basicamente de água, proteínas (albumina, globulinas, fatores de coagulação e outras), carboidratos e lipídios. É completamente congelado até 8 horas após a coleta e mantido, no mínimo, a 18°C negativos, sendo, porém, recomendada a temperatura igual ou inferior a 25°C negativos. Sua validade entre 25°C negativos e 18°C negativos é de 12 meses. Se congelado a temperaturas inferiores a 25°C negativos sua validade é de 24 meses. O congelamento permite a preservação dos fatores da coagulação, fibrinólise e complemento, além de albumina, imunoglobulinas, outras proteínas e sais minerais, e mantém constantes suas propriedades. O componente assim obtido contém = 70UI de Fator VIII/100 ml e, pelo menos, quantidades semelhantes dos outros fatores lábeis e inibidores naturais da coagulação.
A unidade de plasma deve apresentar volume superior a 180 ml, quando utilizado para fins transfusionais, além de não conter anticorpos eritrocitários irregulares de importância clínica. Por convenção, cada ml de PFC tem 1U de atividade de fatores da coagulação.
O plasma isento de crioprecipitado (PIC) é aquele do qual foi retirado, em sistema fechado, o crioprecipitado. Deve ser armazenado à temperatura de, no mínimo, 18°C negativos, sendo, porém, recomendada temperatura igual ou inferior a 25°C negativos. Sua validade é a mesma do PFC e seu volume aproximado de 150 ml a 200 ml. É depletado de FVIII, fibrinogênio e multímeros de alto peso molecular de Fator de von Willebrand, embora contenha a metaloproteinase responsável por sua metabolização.
O plasma de 24 horas (P24) é o hemocomponente separado do sangue total por centrifugação entre 8h e 24 horas após a coleta e congelado completamente, no máximo em uma hora, atingindo temperaturas iguais ou inferiores a 30°C negativos. Deve ser armazenado à temperatura de, no mínimo, 18°C negativos, sendo, porém, recomendada temperatura igual ou inferior a 25°C negativos. Sua validade é a mesma do PFC e seu volume aproximado de 200 a 250 ml. Apresenta uma redução variável de alguns fatores da coagulação em relação ao PFC, principalmente fatores V e VIII.
2.1.4 Crioprecipitado
O crioprecipitado (CRIO) é uma fonte concentrada de algumas proteínas plasmáticas que são insolúveis a temperatura de 1°C a 6°C. É preparado descongelando-se uma unidade de plasma fresco congelado à temperatura de 1°C a 6°C. Depois de descongelado, o plasma sobrenadante é removido deixando-se na bolsa a proteína precipitada e 10-15 ml deste plasma. Este material é então recongelado no período de 1 hora e tem validade de 1 ano.
O crioprecipitado contém glicoproteínas de alto peso molecular (Quadro 1) como de Fator VIII, Fator VIII:vWF (fator von Willebrand), fibrinogênio, Fator XIII e fibronectina. Cada bolsa contém 15 ml de crioprecipitado com aproximadamente 80-150 unidades de Fator VIII; pelo menos 150 mg de fibrinogênio e cerca de 20%-30% (50-75U) do Fator XIII presente na bolsa inicial de PFC. Aproximadamente 40%-70% (100-150U) do fator de von Willebrand presente na unidade inicial de PFC é recuperado no crioprecipitado. A principal fonte de fibrinogênio concentrado é o crioprecipitado.
Quadro 1: Fatores de coagulação e sua meia vida presente numa bolsa de crioprecipitado com volume de 10-15 ml
|
Fatores de coagulação |
Quantidade/bolsa |
Meia-vida (horas) |
|
Fibrinogênio |
150-250 mg |
100-150 |
|
Fator VIII |
80-150U |
12 |
|
Fator von Willebrand |
100-150U |
24 |
|
Fator XIII |
50-75U |
150-300 |
Cada crioprecipitado dever conter no mínimo 80UI de Fator VIII e 150 mg de fibrinogênio e cada pool deve conter os mesmos fatores multiplicado pelo número de bolsas que o compõem. 21
2.1.5 Concentrado de Granulócitos
Os concentrados de granulócitos (CG) são hemocomponentes obtidos por aférese de doador único, por meio de máquinas separadoras de células, de fluxo contínuo ou descontínuo, cujo rendimento de coleta pode ser melhorado pela utilização de doadores estimulados com a administração de fator estimulador de colônias de granulócitos (G-CSF) e corticosteróides.
Cada concentrado deve conter no mínimo 1,0 x 1010 granulócitos em 90% das unidades avaliadas, em um volume final inferior a 500 ml, (geralmente 200-300 ml) incluindo anticoagulante, plasma e também resíduo do agente hemossedimentante utilizado no procedimento de coleta. Além dos granulócitos, usualmente estes concentrados contêm outros leucócitos e plaquetas e cerca de 20-50 ml de hemácias.
Como a função dos granulócitos se deteriora mesmo durante curto armazenamento, os CG devem ser transfundidos assim que possível após a coleta, e, se for inevitável, seu armazenamento deve ser em temperatura entre 20°C e 24°C, em repouso e por, no máximo, 24 horas. Para transporte deste hemocomponente, recomenda-se o uso de recipientes próprios, com produto refrigerante comercial que assegure a manutenção desta temperatura.
O Quadro 2 apresenta os principais hemocomponentes disponíveis como arsenal terapêutico, suas características e temperatura de armazenamento. Cabe destacar que as indicações clínicas para os respectivos hemocomponentes serão objeto dos capítulos seguintes.
Quadro 2: Principais hemocomponentes disponíveis como arsenal terapêutico
|
Hemocomponente |
Formas de obtenção |
Características |
Temperatura de armazenamento |
|
Concentrado de hemácias (CH) |
Centrifugação do sangue total (ST), removendo-se o plasma da massa eritrocitária da bolsa. |
Eritrócitos e pequena quantidade de plasma. Hematócrito: em torno de 70% Volume aproximado: 220/280ml. |
2°C a 6°C. |
|
Concentrado de plaquetas (CP) |
Centrifugação de uma unidade de sangue total ou por aférese de doador único. |
CP obtida de ST: > 5,5 X 1010 plaquetas por bolsa. pH = a 6,4. Volume aproximado 50ml a 60ml CP obtida por aférese: > 3,0 X 1011 plaquetas por bolsa. Volume aproximado: 200ml a 300ml. |
22 ± 2°C, sob agitação constante |
|
Plasma fresco congelado (PFC) |
Centrifugação do sangue total e congelado completamente em até 8 horas depois da coleta do sangue. |
Rico em fatores de coagulação (V, VII e IX) e fibrinogênio Volume aproximado: > 180ml |
18°C negativos. Recomendada 25°C negativos ou inferior. |
|
Plasma isento do crioprecipitado (PIC) |
Plasma do qual foi retirado, em sistema fechado, o crioprecipitado. |
Depletado de FVIII, fibrinogênio e multímeros de alto peso molecular de Fator de von Willebrand, embora contenha a metaloproteinase responsável por sua metabolização. Volume: 150ml a 200ml |
18°C negativos. Recomendada 25°C negativos ou inferior. |
|
Plasma de 24 horas (P24) |
Plasma separado a partir de 1 unidade de sangue total por centrifugação, entre 8h e 24 horas após a coleta, e congelado completamente, no máximo em uma hora, atingindo temperaturas iguais ou inferiores a 30°C negativos. |
Apresenta redução variável de fatores V e VIII, em relação ao PFC. Volume aproximado: 200ml a 250ml |
18°C negativos. Recomendada 25°C negativos ou inferior. |
|
Crioprecipitado (CRIO) |
Fração de plasma insolúvel em frio, obtida a partir do PFC. |
Glicoproteínas de alto peso molecular como de Fator VIII, Fator VIII:vWF (fator von Willebrand), fibrinogênio, Fator XIII e fibronectina. Volume aproximado: 15ml |
18°C negativos. Recomendada 25°C negativos ou inferior. |
|
Concentrado de granulócitos (CG) |
Aférese de doador único. |
Deve conter, no mínimo, 1,0 x 1010 granulócitos. Contém outros leucócitos, plaquetas e cerca de 20ml a 50ml de hemácias. Volume aproximado: 220ml |
Devem ser transfundidos assim que possível após a coleta. Se inevitável, armazenar entre 20°C e 24°C, em repouso, e por, no máximo, 24 horas. |
SOBRE OS DIREITOS AUTORAIS DO DOCUMENTO
Consta no documento:
“Todos os direitos reservados. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer fim comercial.”
O objetivo do site MedicinaNet e seus editores é divulgar este importante documento. Esta reprodução permanecerá aberta para não assinantes indefinidamente.
[1] Aférese é um procedimento caracterizado pela retirada do sangue do doador, seguida da separação de seus componentes por um equipamento próprio, retenção da porção do sangue que se deseja retirar na máquina e devolução dos outros componentes ao doador.