Ceftazidima

Ceftazidima (Injetável) (substância ativa)
Referência: Fortaz (GlaxoSmithKline)
Genérico: assinalado com G
Similar: Kefadim (ABL); Cetaz (União Química)
ceftazidima pentaidratada + carbonato de sódio
(na reconstituição forma-se a Ceftazidima sódica equivalente a Ceftazidima)
Uso injetável
Injetável (pó) 1g: Fortaz; Kefadim (ABL); G
Injetável (pó) 2 g: Fortaz
Armazenagem antes de aberto
Temperatura ambiente (15-30°C).
Proteção à luz: sim, necessária.
Aparência do pó seco: cristalino branco a amarelo-claro.
O que é
antibacteriano [cefalosporina de 3a geração; betalactâmico].
Para que serve
infecção bacteriana por aeróbicos Gram-positivos ou aeróbicos Gram-negativos; infecção bacteriana mista aeróbico-anaeróbico; infecção articular; infecção da pele e dos tecidos moles; infecção intra-abdominal; infecção óssea; infecção urinária; meningite; pneumonia; septicemia; neutropenia febril; infecção por Pseudomonas aeruginosa; infecção por Burkholderia cepacia.
Como age
inibe a síntese da parede celular da bactéria; é bactericida. Biotransformação: não sofre. Eliminação: principalmente urina, como droga inalterada.
Como se usa
Uso injetável – Preparação
Atenção: antibacterianos como as penicilinas e cefalosporinas não devem ser misturados com aminoglicosídeos porque pode haver precipitação desses produtos; se necessário, devem ser administrados em locais diferentes (não misturados numa mesma seringa, frasco ou bolsa); se utilizada a técnica em Y para administração, deve-se suspender temporariamente um produto enquanto se administra o outro. Outras incompatibilidades: consultar informações do fabricante.
Ceftazidima (pó) 1 g – Via intramuscular
Reconstituição
Diluente: Água Estéril para Injeção ou Lidocaína 0,5 ou 1%. Volume: 3 mL.
Atenção: a solução reconstituída desprende gás carbônico, o que aumenta a pressão no interior do frasco; o gás deve ser liberado antes da administração do produto.
Aparência da solução reconstituída: incolor a amarelo-claro logo após a reconstituição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após reconstituição com Água Estéril para Injeção ou Lidocaína 0,5 ou 1%
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8º C): 3 dias.
Administração: em Adultos, nas nádegas (quadrante superior externo); em crianças, na face lateral da coxa.
Atenção: reconstituição com Lidocaína é apenas para injeção intramuscular.
Ceftazidima (pó) 1 g – Via intravenosa direta
Reconstituição
Diluente: Água Estéril para Injeção. Volume: 10 mL.
Atenção: a solução reconstituída desprende gás carbônico, o que aumenta a pressão no interior do frasco; o gás deve ser liberado antes da administração do produto.
Aparência da solução reconstituída: incolor a amarelo-claro logo após a reconstituição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após reconstituição com Água Estéril para Injeção
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8º C): 3 dias.
Tempo de injeção: 3 a 5 minutos.
Ceftazidima (pó) 1 g – Infusão intravenosa
Reconstituição
Diluente: Água Estéril para Injeção. Volume: 10 mL.
Atenção: a solução reconstituída desprende gás carbônico, o que aumenta a pressão no interior do frasco; o gás deve ser liberado antes da administração do produto.
Aparência da solução reconstituída: incolor a amarelo-claro logo após a reconstituição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após reconstituição com Água Estéril para Injeção
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8°C): 3 dias.
Diluição
Diluente: Cloreto de Sódio 0,9%; Glicose 5%. Volume: 50 – 100 mL.
Aparência da solução diluída: incolor a amarelo-claro logo após a diluição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após diluição com Cloreto de Sódio 0,9% ou com Glicose 5%
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8°C): 3 dias.
Tempo de infusão: 30 a 60 minutos.
Ceftazidima (pó) 2 g – VIA INTRAVENOSA DIRETA
Reconstituição
Diluente: Água Estéril para Injeção. Volume: 10 mL.
Atenção: a solução reconstituída desprende gás carbônico, o que aumenta a pressão no interior do frasco; o gás deve ser liberado antes da administração do produto.
Aparência da solução reconstituída: incolor a amarelo-clarologo após a reconstituição; quando armazenada, vai se tornando amarelo mais forte, chegando aamarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após reconstituição com Água Estéril para Injeção
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8º C): 3 dias.
Tempo de injeção: 3 a 5 minutos
Ceftazidima (pó) 2 g – Infusão intravenosa
Reconstituição
Diluente: Água Estéril para Injeção. Volume: 10 mL.
Atenção: a solução reconstituída desprende gás carbônico, o que aumenta a pressão no interior do frasco; o gás deve ser liberado antes da administração do produto.
Aparência da solução reconstituída: incolor a amarelo-clarologo após a reconstituição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade descritos a seguir).
Estabilidade após reconstituição com Água Estéril para Injeção
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8°C): 3 dias.
Diluição
Diluente: Cloreto de Sódio 0,9% ou Glicose 5%. Volume: 100 mL.
Aparência da solução diluída: incolor a amarelo-claro logo após a diluição; quando armazenada, vai se tornando amarelo mais forte, chegando a amarelo-amarronzado (condição normal desde que respeitados os parâmetros de estabilidade – temperatura descritos a seguir).
Estabilidade após diluição com Cloreto de Sódio 0,9% ou Glicose 5%
temperatura ambiente (15 - 30°C): 12 horas.
refrigeração (2-8°C): 3 dias.
Tempo de infusão: 30 a 60 minutos.
Uso injetável – Doses
• doses em termos de Ceftazidima anidra.
Adultos e adolescentes
infecção urinária (não complicada): 250 mg a cada 12 horas.
infecção urinária (complicada): 500 mg cada 8 ou 12 horas. pneumonia (não complicada)
infecção da pele e dos tecidos moles: 500 mg a 1 g a cada 8 horas.
infecção óssea ou articular: 2 g (via intravenosa) a cada 12 horas.
infecção intra-abdominal; infecção pélvica (em mulheres); septicemia; meningite; infecção grave (com risco de vida) (especialmente em paciente imunodeprimido): 2 g (via intra- venosa) a cada 8 horas.
infecção pulmonar (por pseudomonas em paciente com fibrose cística): 30 a 50 mg por kg de peso corporal (via intravenosa) cada 8 horas (até o máximo de 6 g por dia).
Adulto com diminuição da função renal – clearance de creatinina maior que 50 mL/min: mesmas doses de adultos e adolescentes; com clearance de creatinina de 50 mL/minuto ou me- nos, fazer uma dose de ataque de 1 g; a seguir, dose de manutenção em função do clearance de creatinina (em mL/minuto) como abaixo.
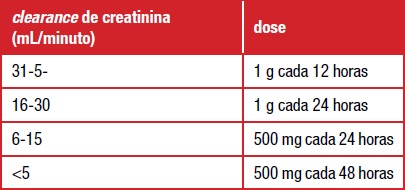
Adulto sob hemodiálise: deve receber uma dose de ataque de 1 g seguido por uma dose de 1 g após cada período de diálise.
Adulto sob diálise intraperitoneal ou diálise peritoneal ambulatorial contínua: deve receber uma dose de ataque de 1 g seguido por uma dose de 500 mg a cada 24 horas.
Idosos
podem exigir diminuição das doses em função da condição renal.
Limite de dose para idosos acima de 75 anos de idade:
1 g a cada 24 horas (mesmo com creatinina normal).
Crianças
meningite
recém-nascido (0 a 4 semanas): 25 a 50 mg por kg de peso corporal, via intravenosa, cada 12 horas.
1 mês a 12 anos: 50 mg por kg de peso corporal, via intravenosa, cada 8 horas.
outras infecções
recém-nascido (0 a 4 semanas): 30 mg por kg de peso corporal, via intravenosa, cada 12 horas.
1 mês a 12 anos: 30 a 50 mg por kg de peso corporal, via intravenosa, cada 8 horas.
Limite de dose para crianças: 6 g por dia.
Criança com diminuição da função renal: a frequência da dose deve ser diminuída em função do grau de diminuição da função renal.
Paciente com diminuição da função do fígado: geralmente é desnecessária a modificação de dose, a menos que haja também diminuição da função renal.
Cuidados especiais
Risco na gravidez:
Classe B
Amamentação:
eliminado no leite em pequena proporção. Problemas não documentados.
Não usar o produto:
reação alérgica prévia a cefalosporina, penicilina e seus derivados ou penicilamina.
Avaliar riscos x Benefícios:
histórico de doença gastrintestinal, particularmente colite ulcerativa, enterite regional ou colite associada a antibiótico (pode ocorrer colite pseudomembranosa); histórico de doença com sangramento (pode ocorrer sangramento por hipoprotrombinemia); diminuição da função renal (usar doses menores).
Reações mais comuns (ocorrem em pelo menos 10% dos pacientes):
Cardiovascular: inflamação na veia; inflamação e obstrução na veia.
Dermatológico: erupção na pele; urticária.
Local da injeção: dor; enduração; abscesso; aumento da temperatura; descamação no local da injeção intramuscular.
Atenção ao utilizar outros produtos.
A ceftazidima:
•pode aumentar o risco de hemorragias com: inibidor da agregação plaquetária; anticoagulante oral; heparina; agente trombolítico.
•pode ter seu risco de causar toxicidade nos rins aumentado por: aminoglicosídeo.
•pode causar efeito antagônico com: cloranfenicol.
Outras considerações importantes
•pacientes com dieta restritiva de sal: considerar que há 2,3 mEq de sódio por grama de produto.
REMÉDIOS COM CEFTAZIDIMA EM SUA COMPOSIÇÃO
• Betazidim• Cefatril
• Cefazima
• Ceftazidon
• Cetaz
• Fortaz
• Intracef
• Kefadim
• Tazidem