Doenças Renais Associadas ao HIV
INTRODUÇÃO E DEFINIÇÕES
No início da década de 1980, foram relatados os primeiros casos de síndrome da imunodeficiência adquirida (AIDS). Desde então, uma série de mudanças ocorreu na epidemiologia dessa doença, em função do surgimento das diversas drogas antivirais e do consequente aumento significativo na sobrevida dos pacientes. Com isto, paralelamente à ocorrência das doenças oportunistas, outras manifestações patológicas passaram a ocorrer na população de pacientes com HIV, como os distúrbios metabólicos, as doenças cardiovasculares e a doença renal.
A associação entre HIV e doenças renais foi primeiramente descrita em 1984, em Miami e Nova York, por investigadores que relataram uma série de casos de pacientes HIV-positivos que desenvolveram proteinúria e perda de função renal, quadro que ficou inicialmente conhecido como nefropatia associada ao HIV (HIVAN). Desde então, muitas outras formas de manifestações clínicas foram descritas. Atualmente,
O espectro das doenças renais em indivíduos infectados pelo HIV é bastante extenso, variando desde quadros de perda aguda de função renal a quadros de perda mais crônica da função, ambos com envolvimento possível dos diversos segmentos renais (vasos, glomérulos, túbulos, interstício) e extrarrenais (alterações volêmicas, doenças do ureter e da bexiga). Sendo assim, a abordagem diagnóstica destes pacientes envolve o conhecimento das principais patologias renais que afetam também indivíduos não infectados pelo HIV, com algumas particularidades a serem discutidas posteriormente.
O desafio consiste em classificar os pacientes em 3 grupos:
1. Perda aguda de função renal (insuficiência renal pré-renal, necrose tubular aguda, nefrite intersticial aguda e outras).
2. Perda crônica da função renal (glomeruloesclerose segmentar e focal (GESF) associada ao HIV, microangiopatia trombótica, glomerulopatias diversas).
3. Distúrbios hidroeletrolíticos e disfunções tubulares (síndrome de Fanconi, hiponatremia, hipercalemia, entre outros).
FISIOPATOLOGIA
Do ponto de vista fisiopatológico, houve um grande avanço no número de evidências sugerindo que a infecção viral direta das células renais pelo HIV-1 é responsável pelo desenvolvimento da doença glomerular, tendo sido identificado HIV-DNA por PCR em células mesangiais, podócitos, túbulos e em leucócitos infiltrantes. As células tubulares renais em pacientes com GESF associada ao HIV funcionam como um reservatório viral, com replicação ativa do HIV independente daquela dos linfócitos do sangue periférico, reforçando a ideia de um papel direto do HIV na patogênese. Recentemente, foi desenvolvido um modelo de rato transgênico que expressa genes do HIV e que apresentou uma glomerulopatia semelhante à nefropatia do HIV. Estes achados sugerem que a expressão de genes virais no tecido renal está envolvida na patogênese da doença renal associada ao HIV. A infecção pelo HIV parece ativar vias apoptóticas celulares envolvidas na patogênese e levar à liberação de várias citocinas, dentre elas TNF-alfa, TGF-beta e interferon.
Além do fator relacionado ao vírus, sugere-se que alguns fatores genéticos possam estar envolvidos na determinação de suscetibilidade do portador de HIV de desenvolver doença renal. Isso se deve ao fato da maioria dos pacientes com envolvimento renal serem negros e apresentarem antecedentes familiares de doença renal crônica.
ACHADOS CLÍNICOS
História Clínica
Durante a avaliação inicial, alguns dados devem ser avaliados na tentativa de orientar o diagnóstico.
Estimativa de Tempo de Doença
No sentido de caracterizar a lesão renal como aguda ou crônica.
Sintomas que Apontem para Hipovolemia
A presença de diarreia, vômitos ou sangramentos importantes são de extremo valor para sugerir a presença de quadro agudo do tipo pré-renal, ou, dependendo do tempo de evolução e da gravidade dos sintomas, até mesmo de uma necrose tubular aguda.
Drogas Utilizadas pelo Paciente
Os pacientes com HIV rotineiramente utilizam drogas nefrotóxicas, tanto para tratamento da doença como das complicações infecciosas, e estas podem estar implicadas na gênese de vários tipos de insuficiência renal aguda (Tabela 1) e toxicidade crônica.
Exposição a Qualquer Outro Agente Nefrotóxico
Além das drogas comumente utilizadas, esses pacientes são expostos a outros agentes nefrotóxicos, como os contrastes radiológicos.
Tabela 1: Drogas comumente associadas ao desenvolvimento de nefrotoxicidade em pacientes HIV-positivo
|
Aciclovir |
Antibióticos lactâmicos |
Ganciclovir |
Quinolonas |
|
Aminoglicosídios |
Etambutol |
Indinavir |
Rifampicina |
|
Anfotericina B |
Fenitoína |
Inibidor da bomba de prótons |
Sulfonamidas |
|
Anti-inflamatórios não hormonais |
Foscarnet |
Penicilinas |
Tenofovir |
Exame Físico
Alguns dados podem ser acrescentados pelo exame físico.
Sinais de Hipovolemia Considerável
A presença de mucosas secas, taquicardia e hipotensão ortostática indicam a possibilidade de um componente pré-renal.
Presença de edema e hipertensão são achados sugestivos de doença renal, embora possam acontecer tanto nos quadros agudos, secundários à hipervolemia, como nos quadros crônicos, secundários à proteinúria e/ou à perda de função renal.
EXAMES COMPLEMENTARES
Alguns exames são necessários na avaliação do envolvimento renal nos pacientes HIV-positivos.
Exames Laboratoriais
Avaliação de Função Renal
São principalmente utilizadas as dosagens séricas de ureia e creatinina. Seu valor é maior se há exames prévios, uma vez que exames recentes normais atestam quadros de insuficiência renal aguda (IRA). Além disso, a razão ureia/creatinina > 40 em portadores de IRA sugere a presença de um componente pré-renal, enquanto o aumento desproporcional de creatinina lembra os quadros de lesão muscular, como a rabdomiólise induzida por drogas.
Sódio Urinário e Fração de Excreção de Sódio e de Ácido Úrico
A presença de sódio urinário > 40 mEq/L e FeNa > 1% e/ou de Fe de ácido úrico > 15% sugere dano tubular nos quadros de insuficiência renal aguda.
Dosagem de Eletrólitos
Dosagens habituais de sódio, potássio, cálcio, fósforo e magnésio são úteis sobretudo nos casos de toxicidade por drogas, sendo clássica a descrição de hipercalemia associada ao uso de trimetoprim, hiponatremia e hipercalemia nos casos de insuficiência adrenal associadas ao HIV, hipocalcemia associada ao foscarnet, e hipofosfatemia, nos casos de síndrome de Fanconi, associada ao uso de tenofovir.
Hemograma e Provas de Hemólise (DHL, Bilirrubinas, Reticulócitos e Haptoglobina)
A presença de achados laboratoriais de anemia hemolítica microangiopática é importante para suspeita de SHU/PTT associada ao HIV. Além disso, nos quadros de insuficiência renal aguda, classicamente não há presença de anemia.
Urina 1
Dentro do grupo das causas de insuficiência renal aguda, a presença de um sedimento normal sugere as causas pré-renais e pós-renais (compressão por tumores e/ou linfonodos, fibrose retroperitoneal, obstrução por coágulos). Várias alterações, entretanto, podem ser encontradas nas causas renais:
presença de hematúria e proteinúria > 1 g em 24 horas: sugerem os quadros glomerulares como a microangiopatia trombótica e as demais glomerulopatias;
leucocitúria com eosinofilúria: sugere nefrite intersticial aguda;
células de descamação epitelial e cilindros pigmentados: favorece necrose tubular aguda e mioglobinúria;
cristalúria: geralmente associada a drogas.
Dentre as causas crônicas, a presença de sedimento urinário anormal é a regra, ressaltando-se que a ausência de hematúria é comum no quadro de glomeruloesclerose segmentar e focal (GESF).
Proteinúria de 24 Horas
A presença de proteinúria em faixas nefróticas (> 3 g em 24 horas) é comumente encontrada na GESF associada ao HIV, tendo sido descrita, entretanto, em casos de microangiopatia trombótica e em alguns casos do grupo das outras glomerulopatias, como a nefropatia da IgA.
Exames de Imagem
1. Ultrassonografia de rins e vias urinárias
Além de auxiliar na exclusão de quadros pós-renais que geralmente cursam com hidronefrose, os dados de tamanho e ecogenicidade são importantes para outros diagnósticos. Os quadros agudos geralmente cursam com rins de tamanho normais sem alterações de ecogenicidade, com exceção da nefrite intersticial aguda que pode cursar com aumento de tamanho e de ecogenicidade. Já os quadros de evolução mais lenta costumam apresentar-se com aumento de ecogenicidade e diminuição de tamanho renal.
2. Tomografia computadorizada
Raramente indicada, auxilia, entretanto, no diagnóstico diferencial entre as causas pós-renais (coágulos, tumores, linfonodos).
Biópsia Renal
As principais indicações de biópsia renal estão listadas na Tabela 2. Pode-se observar que a biópsia renal está especialmente indicada nos quadros com suspeita de envolvimento glomerular. Nos quadros em que esses achados estão ausentes, sugerindo, portanto, envolvimento de túbulo ou interstício, a biópsia renal não é rotineiramente indicada, uma vez que é possível identificar a provável patologia baseando-se nos achados de história e exames laboratoriais (uso de drogas nefrotóxicas, sepse etc.).
Tabela 2: Indicações de biópsia renal
|
Insuficiência renal aguda sem causa clara, principalmente na presença de hematúria e/ou proteinúria |
|
Proteinúria de início recente, particularmente em valores nefróticos (> 3 g) |
|
Hematúria inexplicada, especialmente com cilindros celulares ou função renal anormal |
|
Evidência clínica de microangiopatia trombótica |
|
Doença renal crônica com causa indefinida com qualquer um dos fatores acima ou progressão inexplicada |
|
Glomerulonefrite rapidamente progressiva |
A presença de hematúria e proteinúria >
DIAGNÓSTICO DIFERENCIAL
São muitas as manifestações renais associadas ao HIV, podendo ser agrupadas em 3 grandes grupos: tubulopatias, quadros associados a insuficiência renal aguda e quadros que evoluem com perda crônica de função (DRC). As principais formas de envolvimento renal estão resumidas na Tabela 3.
Tabela 3: Principais formas de acometimento renal em pacientes com HIV
|
IRA pré-renal |
Desidratação |
Sangramento |
|
Diarreia |
| |
|
IRA pós-renal |
Tumores |
Coágulos |
|
Nefrite intersticial aguda |
Antibióticos |
Anti-inflamatórios não hormonais |
|
Rifampicina |
Alopurinol | |
|
Indinavir |
Fenitoína | |
|
Nefropatia por deposição de cristais |
Indinavir |
Aciclovir |
|
Sulfadiazina |
| |
|
Necrose tubular aguda |
Drogas | |
|
Septicemia | ||
|
Tubulopatias |
Tenofovir | |
|
Trimetoprim | ||
|
Anfotericina B | ||
|
Glomerulopatias |
GESF associada ao HIV* |
Microangiopatia trombótica* |
|
GESF clássica |
Amiloidose | |
|
Membranosa |
Nefropatia da IgA | |
|
Glomerulonefrite pós-infecciosa |
Doença por complexo imune relacionada ao HIV* | |
|
Nefropatia por lesões mínimas |
Crioglobulinemia se vírus C associado | |
* Doenças glomerulares diretamente relacionadas ao HIV.
Disfunções Tubulares
Os distúrbios hidroeletrolíticos são comuns em pacientes com infecção avançada pelo HIV. Serão descritos aqui apenas os distúrbios mais frequentes.
Hiponatremia
É observada em até 40% dos pacientes com HIV hospitalizados. Ocorre tanto em situações de hipovolemia, principalmente secundária a perdas gastrintestinais, como de euvolemia no contexto da síndrome da secreção inadequada de ADH (SIADH). Esta última é geralmente secundária a infecção por Pneumocystis carinii, neoplasia maligna ou doença do sistema nervoso central. A insuficiência suprarrenal é uma causa pouco frequente de hiponatremia nesses pacientes. A hiponatremia está associada a aumento das taxas de mortalidade e morbidade, principalmente quando associada a infecções oportunistas.
Hipercalemia
O uso de pentamidina e da combinação sulfametoxazol e trimetoprim está associado ao desenvolvimento de hipercalemia secundária à diminuição da excreção distal de potássio. Num pequeno número de casos, a hipercalemia é secundária à insuficiência suprarrenal.
Síndrome de Fanconi
Alguns pacientes apresentam-se com quadros de fosfatúria, aminoacidúria, glicosúria, além de proteinúria tubular (caracterizado pelo aumento na excreção urinária de beta-2-microglobulina e proteína ligadora de retinol – RBP), característicos de disfunção tubular proximal. É descrita principalmente com o uso de inibidores de transcriptase reversa, análogos de nucleotídios, como o tenofovir, e de nucleosídios, como a lamivudina.
Quadros Associados à Insuficiência Renal Aguda
Várias patologias têm sido descritas nesse grupo ao longo dos anos. As principais são descritas a seguir.
IRA Pré-renal
Poucos dados existem com relação ao desenvolvimento de IRA pré-renal nesses pacientes, entretanto, sabe-se que a presença de vômitos, diarreia e infecções é bastante comum entre eles, predispondo-os a hipovolemia e IRA pré-renal. Os sinais clínicos sugestivos de hipovolemia, como hipotensão postural, taquicardia e mucosas secas, associados a sedimento urinário normal com densidade > 1.015 e/ou osmolaridade urinária > 500 mOsm/kg, além de Na urinário < 20 mEq/L, FENa < 1% e/ou FE ácido úrico < 15% suportam o diagnóstico.
Necrose Tubular Aguda (NTA)
Do ponto de vista etiológico, não difere dos pacientes sem HIV, podendo ser de origem isquêmica (sangramento importante, septicemia) e/ou tóxica, uma vez que esses pacientes são tratados com um grande número de drogas nefrotóxicas, dentre elas aminoglicosídios, pentamidina, anfotericina B, foscarnet, além do uso de drogas ilícitas intravenosas causadoras de rabdomiólise. Os achados de sedimento com células de descamação epitelial, Na urinário > 20 mEq/L, FeNa > 1% e FE ácido úrico > 15% favorecem o diagnóstico de necrose tubular aguda. A mortalidade nesse grupo de pacientes é elevada, mas é comparável a mortalidade de pacientes com necrose tubular aguda sem HIV.
Nefrite Intersticial Aguda (NIA)
A população infectada pelo HIV é exposta a um grande número de medicações, sendo, portanto, suscetível ao desenvolvimento de nefrite intersticial aguda. Num estudo de biópsias renais realizadas em pacientes com HIV, a NIA foi o quarto achado mais comum, seguindo a GESF associada ao HIV, nefropatia hipertensiva e a GESF clássica. As drogas mais comumente envolvidas são as cefalosporinas, drogas que contêm sulfas, quinolonas, inibidor de bomba de prótons e anti-inflamatórios não hormonais.
O tempo de exposição às drogas é variável e a tolerância prévia à droga não a exclui como causa atual da nefrite intersticial. Alguns antirretrovirais estão associados ao desenvolvimento de NIA. Dentre essas, o indinavir é o mais frequentemente descrito como causa de NIA.
A presença de quadro típico com febre, rash e eosinofilia não é habitual, sendo mais comum o achado de IRA com leucocitúria, às custas de eosinófilos, além de hematúria discreta e proteinúria <
Nefropatia por Cristais
Várias medicações podem cristalizar no lúmen tubular, incluindo indinavir, atazanavir, sulfadiazina, ciprofloxacino e aciclovir intravenoso, em função da insolubilidade destas drogas na urina. A depleção de volume com redução do débito urinário é um importante fator de risco para deposição de cristais. Outro fator de risco para a cristalúria são as mudanças no pH urinário, sendo que pH < 5,5 predispõe a precipitação de cristais de sulfa e aciclovir e pH > 6,0 predispõe a formação de cristais de indinavir. O sedimento urinário pode ser normal ou apresentar hematúria discreta.
A incidência de cristalúria com indinavir varia na literatura de 3 a 66% em diferentes séries, com IRA desenvolvendo-se em 9 a 25% dos pacientes. O impacto das complicações renais em pacientes em uso de indinavir é expressivo, sendo responsável por até 33% dos casos de interrupção do uso da droga.
Microangiopatia Trombótica
Inclui a síndrome hemolítico-urêmica (SHU) e a púrpura trombocitopênica trombótica (PTT) e é caracterizada por anemia hemolítica microangiopática e trombocitopenia. Esses distúrbios geralmente têm envolvimento renal com IRA e níveis variáveis de hematúria e proteinúria.
A patogênese permanece desconhecida, acreditando-se resultar de injúria endotelial e deposição de plaquetas na microvasculatura. Infecções coexistentes, citotoxicidade endotelial do HIV, deficiência de inibidores da agregação plaquetária e anormalidades na cascata de coagulação têm sido implicadas.
Os critérios de suspeição diagnóstica utilizados são: presença de perda aguda de função renal e evidências laboratoriais de anemia hemolítica microangiopática (aumento de reticulócitos, presença de esquizócitos, elevação de DHL, redução de haptoglobina) e plaquetopenia. O sedimento urinário é ativo com hematúria e proteinúria, podendo alcançar níveis > 3 g/dL. Em alguns casos, várias formas de envolvimento extrarrenal são descritas, como convulsões, coma, diarreia. A recuperação da função renal ocorre com frequência variável em torno de 50%, sendo o prognóstico pior que nas formas de SHU/PTT idiopáticas, com mortalidade variando entre 66 e 100%.
Quadros Associados à Perda Crônica de Função
GESF Associada ao HIV
Os primeiros casos descritos de doenças renais associadas ao HIV correspondem a casos de GESF que foram classicamente denominados de nefropatia relacionada ao HIV (HIVAN). É a mais comum das nefropatias associadas ao HIV de apresentação crônica em séries de biópsias, embora isso possa representar um viés pela maior realização de biópsias em portadores de proteinúria nefrótica (> 3 g/dL). Nos Estados Unidos, ocorre quase que exclusivamente nos afro-americanos.
Tem sido descrita em todos os estágios de infecção pelo HIV, inclusive no momento da soroconversão. Entretanto, apesar da discussão presente na literatura, a maioria dos trabalhos, geralmente retrospectivos, encontra uma maior frequência em fases mais avançadas da doença, com a maioria dos pacientes já tendo apresentado outras complicações do HIV e contagem de CD4 inferior a 240 células/mm3.
Caracteriza-se clinicamente pela presença de proteinúria, em geral maciça (> 10 g/dia), hipoalbuminemia e perda de função renal, sendo classicamente observada a ausência de edema, hipertensão e hematúria. Os achados ultrassonográficos são de rins de tamanho aumentado com ecogenicidade preservada. Histologicamente, caracteriza-se por glomeruloesclerose segmentar e focal (GESF) associada a dilatações tubulares císticas graves. Os podócitos são hiperplásicos e podem formar pseudocrescentes, com colapso do tufo glomerular. O interstício encontra-se infiltrado por células mononucleares e com edema. Ultraestruturalmente, as células endoteliais glomerulares apresentam inclusões túbulo-reticulares.
A evolução desses casos, se não tratados, é ruim, com progressão para insuficiência renal crônica terminal em 1 a 3 meses. As variáveis associadas com a progressão da doença renal incluem creatinina aumentada ao diagnóstico, baixa contagem de CD4, carga viral elevada, proteinúria maciça e uso prévio de terapia antiviral.
Doença por Complexo Imune Associada ao HIV
Enquanto a glomeruloesclerose segmentar e focal associada ao HIV é mais comum nos pacientes negros, a doença por complexo imune associada ao HIV é mais comum na população branca. Os complexos imunes com antígenos associados ao HIV foram identificados tanto na circulação sanguínea, como no parênquima renal.
Esses pacientes apresentam-se com história de edema, com ou sem perda de função renal e sedimento urinário ativo, além de taxas variáveis de proteinúria e hipertensão arterial. Os achados laboratoriais são semelhantes aos de outras glomerulopatias e a biópsia renal é essencial para o diagnóstico. Dentre estes diagnósticos, predominam a glomerulonefrite membranoproliferativa, a nefropatia da IgA e a forma lúpus-símile. Outros diagnósticos possíveis são: a glomerulonefrite aguda pós-infecciosa, a glomerulonefrite membranosa, a crioglobulinemia, a amiloidose, a doença de lesões mínimas, dentre outros.
Pouco se conhece sobre a patogenia dessas doenças e da relação causal ou não com o HIV. A paucidade de estudos não permite avaliar as diferenças na forma de apresentação com relação ao paciente não HIV, nem há evidências suficientes que suportem estimar diferenças de prognóstico em relação à glomeruloesclerose segmentar e focal associada ao HIV. Entretanto, algumas correlações têm sido encontradas na literatura sugerindo que essas lesões são encontradas com maior frequência entre pacientes brancos, não hipertensos, com maior contagem de CD4, além de apresentar taxa de progressão mais lenta.
Microangiopatia Trombótica
Além de se manifestar com quadro agudo de perda de função renal, conforme já descrito, é também observada em quadros mais insidiosos. Não parece haver diferenças do ponto de vista patogênico, mas a apresentação clínica costuma diferenciar-se pela ausência de sinais laboratoriais evidentes de anemia hemolítica microangiopática. O diagnóstico só é possível com a realização da biópsia renal. A histologia caracteriza-se por depósito de plaquetas e trombo de fibrina em capilares glomerulares, arteríolas e artérias interlobulares, além de edema intimal arteriolar, necrose fibrinoide, mesangiólise e as clássicas lesões arteriolares em “casca de cebola”.
A biópsia renal é fundamental para o diagnóstico das diversas formas de glomerulopatias associadas ao HIV, permitindo também a avaliação do grau de cronicidade e decisão sobre a conduta terapêutica.
TRATAMENTO
Ainda não existem diretrizes que orientem o tratamento das manifestações renais associadas ao HIV e a maioria dos trabalhos envolve número pequeno de pacientes.
GESF Associada ao HIV
Apesar da falta de ensaios clínicos controlados randomizados, o tratamento desta nefropatia tem se baseado em reduzir a replicação viral e lentificar a progressão da doença renal. Dentre as diversas formas de nefropatias associadas ao HIV, esta é a que tem apresentado as melhores respostas de redução na taxa de progressão após a instituição da terapia antirretroviral (HAART). Assim, a presença de glomeruloesclerose segmentar e focal associada ao HIV passou a ser indicação formal de HAART. Também é essencial no tratamento desta glomerulopatia o emprego de drogas bloqueadoras de angiotensina II (inibidores da enzima de conversão de angiotensina ou bloqueadores do receptor AT1 da angiotensina II), conforme já comprovado em estudos clínicos.
O uso de corticoides permanece um tópico de intenso debate na literatura, com estudos mostrando benefícios de redução de proteinúria e retardo da progressão para insuficiência renal. Os esquemas utilizam doses de 60 mg/dia com redução gradual em
Outras Glomerulopatias
Devido à paucidade de estudos para o tratamento das outras glomerulopatias nesses pacientes, a recomendação é a utilização de IECA e HAART, não havendo segurança para utilização de corticoides. Não foi demonstrada correlação clara entre o uso de HAART e o efeito de retardo de progressão de doença renal neste grupo de pacientes.
Microangiopatia Trombótica
Os princípios básicos da terapêutica incluem a infusão de plasma (15 a 20 mL/kg/dia) e/ou a plasmaférese, em adição ao tratamento antirretroviral, embora ainda com sucesso limitado.
IRA Pré-renal, NTA, NIA e Nefropatia por Cristais
As orientações terapêuticas para esses pacientes são semelhantes às dos pacientes não HIV (interrupção da droga, hidratação, correção dos distúrbios eletrolíticos etc.). Faz-se exceção ao uso de corticoides na NIA, uma vez que este tratamento ainda não foi testado em pacientes HIV-positivo.
Tratamento de Pacientes após o Desenvolvimento de Doença Renal Crônica Terminal
Terapia de Substituição Renal
A partir da década de 1990, os avanços no tratamento da infecção viral e a melhora no manuseio de outras condições próprias do paciente em diálise (anemia, hiperparatireoidismo) permitiram uma melhora expressiva na sobrevida de pacientes HIV-positivo
Transplante Renal
A maioria dos centros de transplante renal não tem incluído pacientes HIV-positivo em sua rotina e, portanto, pouco se conhece a evolução destes pacientes a curto e longo prazos, assim como os efeitos da imunossupressão. Alguns centros têm relatado séries pequenas, sugerindo segurança e eficácia nesta modalidade de tratamento, mas ainda não existe consenso na literatura.
O tratamento das glomerulopatias associadas ao HIV baseia-se essencialmente na instituição de HAART e emprego de IECA ou BRA. A microangiopatia trombótica deve ser tratada com o emprego de plasma fresco e/ou plasmaférese. A terapia de substituição renal já é oferecida a estes pacientes com segurança, sem que haja ainda consenso na literatura em relação ao transplante renal.
ALGORITMO
Algoritmo 1: Avaliação de paciente HIV-positivo com envolvimento renal.
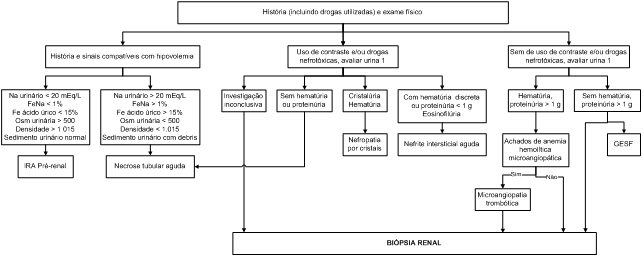
BIBLIOGRAFIA
1. Daugas E, Rougier JP, Hill G. HAART-related nephropathies in HIV-infected patients. Kidney Int 2005; 67:393-403.
2. Fine DM, Perazella MA, Lucas GM, Alta MG. Kidney biopsy in HIV: beyond HIV-associated nephropathy. American Journal of Kidney Diseases 2008; 51:504-14.
3. Kumar MSA, Sierka DR, Damask AM, et al. Safety and success of kidney transplantation and concomitant immunossupression in HIV-positive patients. Kidney Int 2005; 67:1622-29.
4. Perazella MA. Drug-induced nephropathy: an update. Expert Opin Drug Saf 2005; 4:689-706.
5. Rao TKS. Human immunodeficiency virus infection and renal failure. Infect Dis Clin North Am 2001; 15:833-50.
6. Ross MJ, Klotman PE. Recent progresss in HIV- associated nephropathy. J Am Soc Nephrol 2002; 13:2997-3004.
7. Rossert J. Drug-induced acute interstitial nephritis. Kidney Int 2001; 60:804-17.
8. Szczech LA, Gupta SK, Habas R, et al. The clinical epidemiology and course of the spectrum of renal diseases associated with HIV infection. Kidney Int 2004; 66:1145-52.
9. Vigneau C, Guiard-Schmid JB, Tourret J, et al. The clinical characteristics of HIV-infected patients receiving dialysis in France between 1997 and 2002. Kidney Int 2005; 67:1509-14.
10. Weiner NJ, Goodman JW, Kimmel PL. The HIV-associated renal diseases: current insight into pathogenesis and treatment. Kidney Int 2003; 63:1618-31.